Люминальный тип рака молочной железы: фенотип опухоли
Это
только сначала кажется сложным и непонятным. Столкнувшись с врагом лицом к
лицу, пациентки быстро начинают разбираться в медицинских аббревиатурах. Люминальный
тип рака молочной железы разделятся на 3 подтипа:
- A – выявляется
достаточное количество РЭ и РП, негативный HER2,
низкий Ki-67; - B HER2- есть положительные РЭ и РП, негативный HER2, но Ki-67 превышает
14%; - B HER2+ обнаружено достаточно РЭ и РП, но положительный HER2 и любое значение Ki-67.
Первый
вариант является самым оптимальным из зол: в процессе лечения можно ожидать
хорошую реакцию опухоли на препараты, потому что есть рецепторы к стероидам
(гормонотерапия будет давать лучший эффект, чем химиотерапия). Если мало HER2 и низкая пролиферативная активность, то
агрессивность опухолевой ткани невысока, а, значит, риск раннего метастазирования
ниже.
При
HER2+ раковые клетки имеют много шансов для быстрого
роста, а высокий индекс пролиферации указывает на вероятность быстрого
увеличения массы опухолевой ткани.
Диагностика
Для постановки точного диагноза необходима консультация у маммолога, который назначает ряд обследований. Для начала проводят ультразвуковое исследование, магниторезонансную томографию и маммографию, что позволяет дифференцировать инвазивную карциному неспецифического типа, поскольку симптоматика схожа.
УЗИ считается наиболее информативной мерой, которая не несет опасности для пациентки. Такая методика дает возможность определить заболевание на первоначальных этапах формирования, при этом назначается необходимая терапия. Для более точной картины назначается томография очага поражения.
Для выяснения типа новообразования осуществляется биопсия пораженной ткани, забор материала проводится посредством специальной иглы. Подобная процедура выполняется под местным обезболиванием (анестезией). Далее полученный материал проходит иммуногистологическое и химическое исследование в лабораторных условиях.
Проведение процедуры заключается в определении наличия вероятных целей для использования терапевтических мер. Также выявляется присутствие выработки женских половых гормонов рецепторами, помимо этого, определяется повышенная активность белка Her2 и быстрота деления патологических клеток.
Прогестерон и эстроген – это женские гормоны, которые контролируют состояние организма в период полового созревания, менопаузы, регулируют менструальный цикл, вынашивание беременности, роды.
Если после проведения всех исследований обнаруживается выработка этих гормонов, то это указывает на гормонапозитивную патологию, при ее отсутствии – на гормонально-негативную.
Что представляет собой люминальный рак груди?
Рак молочной железы представлен широким рядом специфических и отличающихся между собой по происхождению, особенностям клинического течения, восприимчивости к лечению, опухолей. При этом даже одинаковые по строению злокачественные новообразования могут происходить из разных групп клеток. Благодаря наличию методов генетической экспрессии (определения генетических особенностей рака) и сопоставлению полученных данных с клинической картиной, восприимчивостью опухоли к лечению и т. д. можно выделить несколько групп РМЖ.
Каждая из групп опухолей молочной железы имеет свои клетки-предшественницы, с которых она развилась, индивидуальные особенности клеточного и молекулярного строения, что влияет на прогноз течения болезни и проводимое лечение. Согласно методикам определения групп злокачественных новообразований, основанные на их иммунологической и гистологической структуре, восприимчивости раковых клеток к эстрогенам и прогестерону, рецептору эпидермального роста типа 2 (hеr2/neu), выделяют следующие типы рака груди:
- люминальный тип а молочной железы;
- люминальный тип b рака молочной железы;
- her2+ рак грудной железы;
- triple negative рак груди или же трижды отрицательный рак.
Люминальным раком груди считается опухоль, имеющая на поверхности своих клеток рецепторную систему к эстрогену и прогестерону. А в зависимости от чувствительности к рецептору эпидермального роста типа 2 люминальные опухоли разделяют на тип а и тип b. Первые не чувствительны к 2 виду рецептора эпидермального роста, вторые – обладают выраженной чувствительностью к нему.
Резистентность первичная (de novo) и вторичная (приобретенная)
Несмотря на то что эндокринотерапия является основным видом лечения больных диссеминированным РЭ+ РМЖ, получить ответ на проводимое лечение удается не во всех случаях. Речь идет о развитии первичной (de novo) или вторичной (приобретенной) резистентности к проводимой ранее гормонотерапии, в ряде случаев являющейся вполне обоснованной причиной отказа от продолжения гормоно- и начала химиотерапии.
Механизм резистентности к гормонотерапии может быть объяснен тем, что функцию заблокированных РЭ на поверхности клетки могут взять на себя альтернативные нижележащие сигнальные пути, в частности внутриклеточный сигнальный каскад PI3K/AKT/mTOR. Субстрат комплекса mTORC1 фосфорилирует внутриклеточный домен AF-1 РЭ, который отвечает за не зависимую от лиганда активацию рецептора. Таким образом, альтернативная активация РЭ может способствовать развитию резистентности к эндокринотерапии . Это явилось теоретической предпосылкой к изучению эффективности ингибитора mTOR эверолимуса для больных диссеминированным РЭ+ РМЖ, резистентных к гормонотерапии.
Люминальный рак молочной железы
Как и злокачественная опухоль любой другой локализации, рак молочной железы имеет разные типы
Определить биологический тип опухоли жизненно важно для пациента, от этого зависит чувствительность опухолевых клеток к препаратам и исход лечения. . В группе риска — женщины старше 39 лет и пациентки, имеющие в анамнезе разбалансировку гормонального фона.
В группе риска — женщины старше 39 лет и пациентки, имеющие в анамнезе разбалансировку гормонального фона.
Три типа люминального рака — три разных стратегии лечения?
При любом подтипе люминального рака молочной железы назначается хирургическое вмешательство. Это — залог благоприятного прогноза. Если молочная железа не удаляется полностью, то после хирургического вмешательства онкологи предписывают облучение, чтобы исключить повторное появление и разрастание опухоли.
Люминальный рак молочной железы — тип злокачественной опухоли, который зависит от гормонов эстрогена и прогестина. Раковые клетки такой опухоли имеют специальные рецепторы, которые при соприкосновении с гормонами дают сигнал к делению. В результате опухоль растет. Такой тип опухоли называют люминальным А типом.
При люминальном А типе пациент получает тамоксифен. Этот препарат служит “колпачком” для рецепторов опухолевых клеток и не дает им соприкасаться с гормонами и препятствует тем самым делению клеток. При метастазах дополнительно назначаются эндокринные препараты, при множественном метастазировании — химиотерапия.
При люминальном В типе кроме чувствительности к гормонам специалисты учитывают наличие/отсутствие гена HER-2, который помогает опухоли не реагировать на вводимые препараты или успешно от них защищаться.
Даже при HER-2-негативном типе пациентам с таким типом опухоли предлагается химиотерапия. В этом случае схема лечения выглядит как операция — химиотерапия — гормональная терапия.
HER-2-позитивный подтип имеет самый неблагоприятный прогноз. Здесь онкологи в сочетании с химиотерапией и гормонотерапией применяют таргетную терапию, чтобы прекратить подачу сигнала на деление клеток. Для таргетной терапии используется трастузумаб.
В составе тюменского медицинского кластера Medical City находится крупнейший на территории Уральского федерального округа онкологический центр с собственными радиологическим и морфологическим центрами, центром лучевой диагностики, тремя маммологическими центрами и центром женского здоровья.

Мы приглашаем Вас на лечение и предлагаем комплексные программы медицинского туризма: Medical City возьмет на себя заботы об организации Вашего трансфера, лечения, проживания и реабилитации. В реабилитационный период Вас ждет культурная программа с погружением в сибирскую культуру и легендарные места.
Прогноз
По статистическим данным, лечебная тактика дает хороший эффект, но остается большой риск рецидива. При правильной терапии и высоком иммунитете пациентки можно добиться хороших результатов и благоприятного прогноза.
Большая выживаемость наблюдается при диагностировании типа А. Тип В устранить практически не удается, поэтому терапия направлена на снижение проявления симптомов и продление жизни.
Реабилитационный период после хирургического вмешательства долгий, проходить его нужно под врачебным контролем, с соблюдением всех его рекомендаций. При этом не исключено полное излечение от патологии.
Радиотерапия рака молочной железы на стадиях I, IIA
Грудь и грудная стенка
После органосохраняющей операции показано проведение радиотерапии, целевой областью которой является вся оставшаяся после операции грудь, а также прилегающая грудная стенка. Как показали последние клинические исследования, такая адъювантная радиотерапия позволяет снизить риск локального рецидива у пациенток со статусом N0 с 31% до 19,6%, у пациенток со статусом N+ — на 21,2%. Существует два метода адъювантной радиотерапии после органосохраняющей операции:
- Конвенциональная — 50 Гр (25 сеансов в течении 5 недель).
- Гипофракционная — 40-42,5 Гр (15–16 сеансов в течении 3 недель).
Ложе опухоли (Boost)
Дополнительное Boost-облучение ложа опухоли 10–16 Гр значительно уменьшает вероятность возникновения локального рецидива.
Момент проведения адъювантной лучевой терапии
Пациенткам без показаний к проведению адъювантной химиотерапии рекомендовано начать радиотерапию через 4–6 недель после операции. При комбинированной радиохимиотерапии лучевая терапия проводится после химиотерапии, но не позже, чем через 7 месяцев после операции.
Частичное облучение груди (интраоперационная радиотерапия IORT).
Интраоперационная радиотерапия (IORT)
Интраоперационная радиотерапия (IORT) — метод лучевой терапии, который проводится во время операции по резекции опухоли для облучения высокой дозой ее ложа и маргинальных краев резекции.
Подробнее о процедуре →
Альтернативой адъювантного облучения является интраоперационная радиотерапия, при которой еще во время операции облучается ложе опухоли с помощью специального аппликатора в течении 20–45 минут дозой 20 Гр. Преимуществом IORT является уменьшение лучевой нагрузки и сокращение срока локальной терапии.
Механизм действия инновационного таргетного анти-mTOR препарата эверолимус
Эверолимус является избирательным ингибитором серин-треониновой киназы mTOR (мишени рапамицина у млекопитающих), важнейшего регулятора синтеза белка в дистальной части PI3K/AKT-зависимого каскада, деятельность которого нарушена в большинстве опухолевых клетках человека. Эверолимус проявляет свою активность за счет высокоаффинного взаимодействия с внутриклеточным рецепторным белком FKBP12. Комплекс FKBP12-эверолимус связывается с mTORC1 и ингибирует его способность к передаче сигналов. Блокировка трансляции основных протеинов, участвующих в регуляции клеточного цикла, гликолиза и адаптации клеток к гипоксии, ведет к подавлению роста и ангиогенеза опухоли . Итак, таргетный анти-mTOR-препарат эверолимус является активным ингибитором передачи пролиферативного сигнала к делению опухолевых клеток, росту кровеносных сосудов и метаболизму клеток. Но проявится ли его биологическое направленное действие по отношению к гормонозависимому РМЖ, резистентному к нескольким линиям лекарственного лечения, включающего эндокринотерапию?
Симптомы
Для своевременного выявления раковой патологии и назначения соответствующего эффективного лечения, требуется точно определить симптомы, которые характерны именно для раковых опухолей молочной железы:
- Различные изменения в области сосков. Новообразование способно изменить форму сосков, приводит к их втягиванию, отечности.
- Болевой синдром, который усиливается во время пальпации. Появляются неестественные выделения, которые со временем начинают приобретать неприятный запах. На начальных стадиях появляются только при надавливании, далее вытекают самопроизвольно, без механического воздействия.
- Дискомфортные ощущения и боль в области подмышек при поднятии рук вверх.
- Наличие уплотнений в области грудной железы, ощущается при пальпации, можно выявить самостоятельно при прощупывании. Именно поэтому рекомендуется регулярно проводить профилактическое обследование у специалиста, а также в домашних условиях.
- Утрата прежней формы, это сильно заметно на запущенных стадиях патологии. При этом сосок втягивается, нередко наблюдаются ямочки и прочие нарушения структуры груди.
- Изменение кожного покрова, который обретает аномально розовый либо бордовый оттенок. Нередко наблюдается шелушение, зуд, мелкие трещинки.
При появлении подобных признаков, необходимо срочно обратиться к специалисту в области онкологии либо маммологии. Подобное отношение увеличивает шансы пациентки на устранение заболевание и продление ее жизни.
Лечебная тактика
Оценив молекулярный подтип опухоли, врач назначит терапию. На первом этапе люминальный рак (подтип A) можно смело лечить гормональными и химиотерапевтическими препаратами – положительный эффект будет обязательно. При подтипе B HER2- лучше использовать только химиотерапию, а гормоны применять в послеоперационном периоде. При подтипе B HER2+ оптимальны химия и таргетная анти-her2 терапия.
После хирургической операции и курсов лучевой терапии надо продолжить лекарственную терапию
Люминальный тип рака молочной железы хорошо поддается гормонотерапии, но важно всегда учитывать значение HER2 (позитивное или негативное), чтобы по показаниям применять таргетные препараты
По статистике, люминальный тип рака молочной железы выявляется у большинства пациенток 60-75% (более 40% подтип A, более 20% – подтип B HER2-), что позволяет надеяться на положительный результат комплексной терапии.
Профилактика
Предупредить возникновение патологии возможно, если устранить все провоцирующие причины. Важным аспектом считается контроль над собственным весом, соответственно за рационом питания, вести здоровый образ жизни. Избегать различных травм области груди, сильных стрессовых ситуаций.
При возникновении первичных проявлений необходимо сразу обратиться за консультацией к врачу для подтверждения либо опровержения подозрений, рекомендуется периодически проходить маммограф, за направлением необходимо обратиться к маммологу.
Соблюдение профилактических мер не всегда дает возможность устранить риск формирования раковых клеток, в таких ситуациях необходимо провести своевременную терапию, что даст возможность улучшить прогноз на выживание.
Звучит красиво – «цифровая экосистема»
Фундамент будущего цифрового здравоохранения еще в 2011 году с утверждения концепции единой государственной информационной системы в сфере здравоохранения (ЕГИСЗ). А через несколько лет Минздрав России презентовал федеральный проект «Создание единого цифрового контура (ЕЦК) в здравоохранении на основе ЕГИСЗ». Срок реализации проекта – 2019–2024 годы, консолидированное финансирование проекта оценивается в 177 млрд руб.
Так называемая цифровая экосистема здравоохранения предполагает не только объединение всех потоков медицинской информации в ЕГИСЗ, но и появление большого количества сервисов для медицинского сообщества и пациентов: электронный документооборот, телемедицинские технологии, электронная запись к врачу, оформление электронных рецептов и автоматизированное управление льготным лекарственным обеспечением, программы поддержки принятия врачебных решений и т. д.
Благодаря всем этим техническим инновациям, как указывает регулятор, будет обеспечено «повышение эффективности функционирования системы здравоохранения».
Правильные цели, верные задачи. А что мы имеем на пятом году работы над решением этих задач?
Методы лечения
При использовании традиционных способов лечения осуществляется определённое воздействие и на раковые структуры, и на здоровые клетки. В устранении болезни обычно применяется комплексное лечение, включающее резекцию очага новообразования.
Основными методами лечения рака молочной железы являются:
- таргетная терапия
- воздействие химиопрепаратами
- лучевая терапия
- радикальная хирургия
- гормональная терапия
Гормональная и таргетная терапия
Наибольшую эффективность в устранении люминального подтипа рака показывает гормональная терапия. Позитивный настрой самого пациента и надежда на выздоровление также играют важную роль. Лечить болезнь требуется комплексно. Наиболее эффективное влияние оказывают ингибиторы ароматазы и препарат Тамоксифен.
Люминальный рак тип В эффективно лечится медикаментом Трастузумаб. Медикамент относится к группе высокоэффективных противоопухолевых средств и содержит моноклональные антитела. Попадая в организм, компоненты лекарства вступают во взаимодействие с внутриклеточным доменом определённых белковых соединений, вызывающих размножение патологических клеток. Препарат активно подавляет рост злокачественной опухоли и тормозит процесс ее развития. Монотерапия Трастузумабом возможна также при появлении метастаз. Препарат прекращает питание злокачественных клеток и положительно влияет на самочувствие пациента.
Таргетная терапия базируется на новейших достижениях в области иммунологии и помогает победить рак даже при отрицательном прогнозе. Она вызывает быструю гибель поражённой клетки и отличается отсутствием явно выраженных побочных эффектов. Таргетные медикаменты применяются как в комплексе с другими средствами, так и в качестве монотерапии.
Лекарства воздействуют непосредственно на наружные и внутриклеточные рецепторы и белковые соединения, которые вызывают развитие образования. Белок продуцирует опухолевые клетки и вызывает разрастание кровеносных сосудов около новообразования. Таргетная терапия разрушает различные биохимические цепочки, которые способствуют развитию опухоли.
К эффективным таргетным препаратам относятся селективные модуляторы эстрогеновых рецепторов – Герцептин, Аромазин, Аримидекс. Они понижают уровень синтеза эстрогенов и активность ароматазы, подавляют жизнедеятельность раковых клеток.
Химиотерапия и лучевая терапия
Химиотерапия назначается в очень редких случаях, когда показатель Ki-67 достаточно высок. При данном виде лечения препараты оказывают на раковые клетки цитотоксическое воздействие. Они угнетают размножение злокачественных клеток.
Лучевая терапия заключается в рентгеновском излучении патологического очага. Ионизирующая радиация воздействует на опухолевые структуры и разрушает их. Метод может использоваться до или после операции, вместе с химиотерапией, а также, как самостоятельный. Лучевая терапия помогает добиться хорошего результата лечения.
Хирургическая операция
Вылечивать заболевание можно и хирургическим путём. Это достаточно инвазивный и сложный метод. Поражённый перерождёнными клеточными структурами участок удаляется. В некоторых случаях молочная железа удаляется полностью. Вырезаются также соседние лимфоузлы. Извлечение поражённых тканей выполняется квалифицированным хирургом под общей анестезией.
Причины
Этиология возникновения патологии до сих пор до конца не выявлена. Однако благодаря тщательному изучению репродуктивного анамнеза доказано влияние определенных факторов на возникновение люминарного рака молочной железы:
- Отсутствие беременности — женщина никогда не рожала.
- Поздняя первая беременность – первые роды после 28 лет.
- Раннее начало первой менструации – раньше 12 лет.
- Позднее наступление менопаузы – после 50-55 лет.
- Раннее начало половой жизни у девочек – первый сексуальный опыт ранее 12 лет.
- Нарушение на гормональном уровне – сбой в организме наблюдается на фоне бесконтрольного приема оральных противозачаточных препаратов.
- Возрастное старение организма – статистика показывает, что риск возникновения заболевания возрастает уже после 30 лет. Практически у 90% пациенток болезнь была диагностирована после 40 лет.
- Нездоровое питание – регулярное использование продуктов, которые содержат много холестерина, а также жирных блюд, вызывает возникновение раковых клеток в молочной железе.
- Отсутствие половой жизни на протяжении нескольких лет, нерегулярные половые контакты.
- Предшествующие аборты, медицинское прерывание беременности до первых родов.
- Сопутствующие болезни – миома матки; мастопатия – фиброзно-кистозное доброкачественное заболевание молочной железы, характеризующееся аномальным разрастанием тканей, болевым симптомом, патологической секрецией; другие нарушения репродуктивных органов.
- Пережитые травмы груди.
- Вредные привычки – злоупотребление алкогольными напитками, табачными изделиями.
- Неблагоприятные условия труда – регулярный контакт с различными химикатами, токсинами.
Существенную роль оказывает наследственная предрасположенность пациентки. Если у близких родственников диагностировалась подобная патология, то риск развития заболевания существенно увеличивается.
Биологические подтипы рака молочной железы
Биологический подтип определяется наличием или отсутствием определенных рецепторов на поверхности или внутри опухолевых клеток. Рецепторы — своеобразные “антенны” для коммуникации клеток друг с другом. Чтобы их обнаружить, врач-патоморфолог проводит иммуногистохимическое исследование ткани опухоли, обрабатывая ее специальными красителями. Возможно проведение и других исследований, например, цитогенетических или молекулярно-генетических. Современное лечение рака молочной железы невозможно без определения биологического подтипа, поскольку он во многом определяет тактику лечения.
Как определяется биологический подтип?
Учитывается наличие на поверхности или внутри клеток опухоли рецепторов эстрогена, прогестерона и эпидермального фактора роста типа 2 (HER2), а также количество активно размножающихся клеток (ki-67).
Рецепторы эстрогена и прогестерона — это структуры, которые активируются при присоединении к ним молекул гормонов эстрогена или прогестерона соответственно. Если в опухоли в большом количестве присутствуют такие рецепторы, запускаются процессы роста и бесконтрольного размножения опухолевых клеток. В этом случае врачи обычно назначают гормональную терапию, которая уменьшает активацию гормональных рецепторов и тормозит деление опухолевых клеток.
HER2 (Human epidermal growth factor receptor 2 / рецептор эпидермального фактора роста тип 2) — в норме присутствует на многих клетках покровных тканей и его активация также запускает деление клеток. Иногда может в большом количестве присутствовать на клетках опухоли молочной железы. В этой ситуации эффективна таргетная терапия специальными препаратами, которые избирательно блокируют эти рецепторы и не позволяют опухолевым клеткам размножаться. Более подробно о лечении HER2-позитивного рака читайте здесь.
Активность деления клеток оценивается при помощи показателя Ki67. Это белок, который есть в клетках только в тот момент, когда они активно участвуют в размножении. Чем выше этот показатель, тем активнее делятся опухолевые клетки. Клиническое значение его неоднозначно: с одной стороны, рак молочной железы с более высоким показателем Ki67 имеет менее благоприятные прогнозы, с другой, такие опухоли лучше реагируют на лечение при помощи химиотерапии.
В настоящее время принято выделять следующие подтипы в зависимости от обнаружения описанных выше признаков.
| HER2 | Рецепторы эстрогена | Рецепторы прогестерона | Ki67 | |
| Люминальный А | Отсутствие HER2 | Позитивные рецепторы эстрогена | Много рецепторов прогестерона (>20%) | Низкий показатель Ki67 (<20%) |
| Люминальный Б HER2-негативный | Отсутствие HER2 | Позитивные рецепторы эстрогена | Мало рецепторов прогестерона (<20%) или высокий показатель Ki67 (>30%) |
|
| Люминальный Б HER2-позитивный | Позитивные рецепторы HER2 | Позитивные рецепторы эстрогена | Любой показатель | Любой показатель |
| HER2-позитивный | Позитивные рецепторы HER2 | Отсутствие рецепторов эстрогена | Отсутствие рецепторов прогестерона | Любой показатель |
| Трижды-негативный | Отсутствие HER2 | Отсутствие рецепторов эстрогена | Отсутствие рецепторов прогестерона | Любой показатель |
Люминальный А подтип является наиболее распространенным и имеет наиболее благоприятный прогноз, в то время как трижды-негативный характеризуется относительно неблагоприятным прогнозом и может быть связан с наличием BRCA мутации.
Люминальный рак молочной железы
Люминальный рак молочной железы развивается во внутренних, или просветных, клетках. Эти клетки выстилают молочные протоки. Люминальный рак включает один тип гормонального рецептора.
Существует два типа люминального рака молочной железы: люминальный A (LA) и люминальный B (LB).
Ключевое различие между этими двумя типами заключается в том, что LA-клетки содержат меньше белка Ki-67. Этот белок контролирует скорость роста опухолевых клеток. Таким образом, рак LA растет медленнее, чем рак LB, и у него лучший прогноз.
Люминальный рак молочной железы А
Согласно некоторым исследованиям, около 30-45% случаев рака молочной железы приходится на LA.
Рак LA имеет следующие характеристики:
- Клетки являются HER2-отрицательными
- Клетки дают положительный результат на рецепторы эстрогена
- Низкие уровни Ki-67
- Опухоли низкой степени злокачественности
Люминальный рак молочной железы В
По некоторым оценкам, 10–20% случаев рака молочной железы являются LB-раком молочной железы. Рак LB может быть как HER2-отрицательным, так и HER2-положительным. Он имеет следующие характеристики:
- Клетки дают положительный результат на рецепторы эстрогена
- Высокие уровни Ki-67
- Опухоли более высокой степени злокачественности
- Большие опухоли
- Высокая вероятность распространения на лимфатический узел
Характер люминального типа B рака молочной железы
Иначе выглядит люминальный b тип заболевания. Этот подвид раковой опухоли способен давать метастазы и действует негативно на функции лимфоузлов. Болезнь диагностируется редко – среди всех онкозаболеваний составляющая болезни равна всего лишь 10%. Чаще болеют люминальным раком В молодые девушки и женщины в пременопаузе.
Протекает болезнь тяжело и с характерными особенностями. При развитии опухоли наблюдается положительная чувствительность к гормональным веществам
Важно определить заболевание на ранней стадии – при несвоевременной диагностике люминального рака молочной железы типа В и поздно начатой терапии прогноз медиков неутешителен
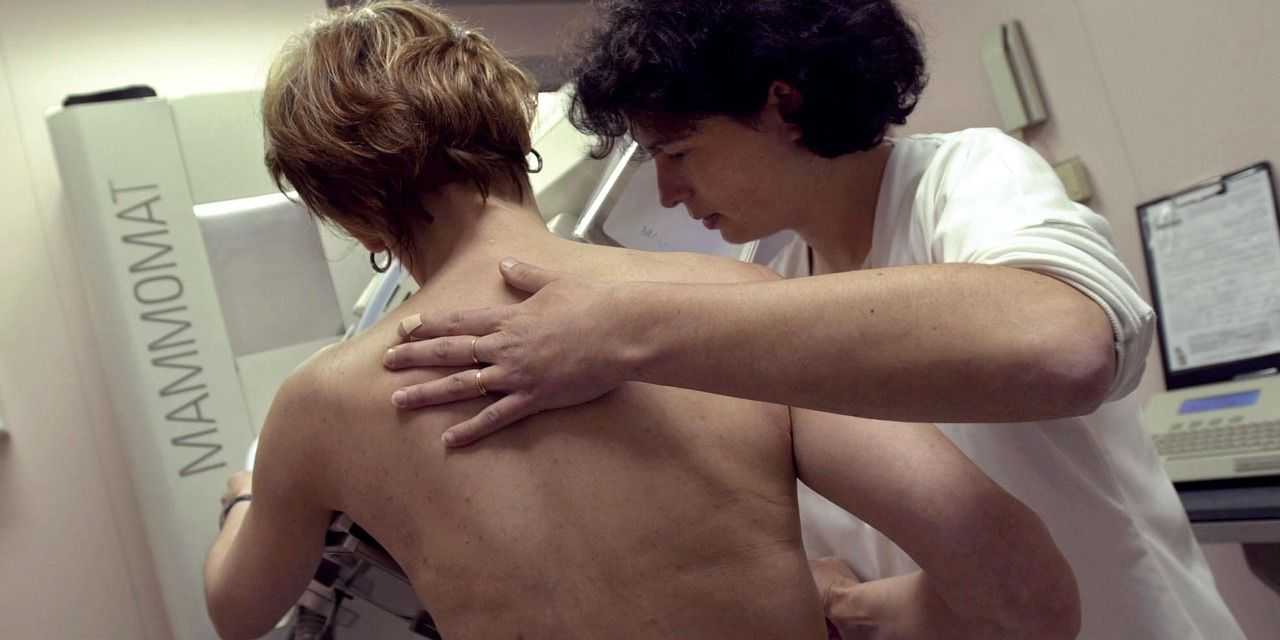
Диагностика и дифференциация
Биология клеток рака молочной железы определяется при генетическом тестировании или ИГХ анализе. Генетическая классификация опухоли не обещает абсолютно одинакового течения заболевания, но помогает подобрать оптимальное лечение, что невозможно сделать с учётом одной только морфологии.
Гистологическое исследование показывает степень захвата злокачественными клетками ткани молочной железы и близлежащих лимфоузлов, позволяет косвенно отследить вероятность раннего метастазирования. Рентген, КТ и МРТ, УЗИ и ПЭТ помогут найти метастазы, но только молекулярный анализ выберет оптимальную терапию.
Любой люминальный вариант рака молочной железы предполагает чувствительность к эндокринному воздействию, но не исключает и позитивную реакцию на химиотерапию, а при наличии гена НЕR2 противоопухолевая эффективность повышается таргетным трастузумабом. Сочетание гормонотерапии с таргетным препаратом пока не стало рутиной, но и не исключается.

Группы риска
Люминальный В her2-негативный или люминальный тип А карциномы развивается не сам по себе, а вследствие гормональной разбалансировки. Вне зависимости от гормонального фона все женщины старше 39 лет считаются группой риска и каждые 24 месяца нуждаются в маммологическом обследовании.
Высока вероятность развития РМЖ у женщин из семей, где уже были карциномы органов репродуктивной системы и толстой кишки, поэтому им необходимо пройти генетическое обследование на гены BRCA. Среди всех злокачественных заболеваний груди группа наследственных раков немногочисленна — 3-5%.
Важным фактором риска признается очень плотная ткань железы, что легко выявляется при маммографии. При возрастании плотности с 5% до 75% вероятность карциномы усугубляется вчетверо. Кроме того, при высокой плотности сложно найти ранние негативные изменения.
Симптомы и признаки
Клинические проявления люминального рака ничем не отличаются от симптомов, сопровождающих другие биологические типы РМЖ: такие же внешние признаки опухоли, те же лимфатические коллекторы и зоны метастазирования.

При люминальном раке используется стандартная градация по системе TNM, аналогично распределение по стадиям, но есть отличие в прогнозе заболевания. Люминальные подтипы протекают лучше остальных и наиболее благоприятен тип А с индолентным, то есть неагрессивным развитием. При прочих равных условиях именно в этой подгруппе фиксируется максимальная выживаемость, но онкологическая статистика пока не учитывает выживаемость в зависимости от молекулярно-генетического типа.
Особенности люминального типа А рака молочной железы
Данный вид рака имеет своё отличие – негативную экспрессию определённых рецепторов к прогестерону и эстрогену. При развитии опухоли полиферативная активность составляет меньше 19%. Риск осложнений и рецидивов при грамотно назначенном лечении сводится к минимуму.
Отличительные особенности данного вида рака:
- высокая либо умеренная гормональная чувствительность
- отрицательная гиперэкспрессия HER2
- положительные РП и РЭ
- сниженный показатель Ki-67
Повышенная чувствительность новообразования вида А указывает на то, что злокачественные структуры опухоли станут реагировать на введение гормональных препаратов. Люминальный тип является гормонозависимым. Терапия рака в такой ситуации направляется на блокировку гормональных рецепторов и разрушение их синтеза.
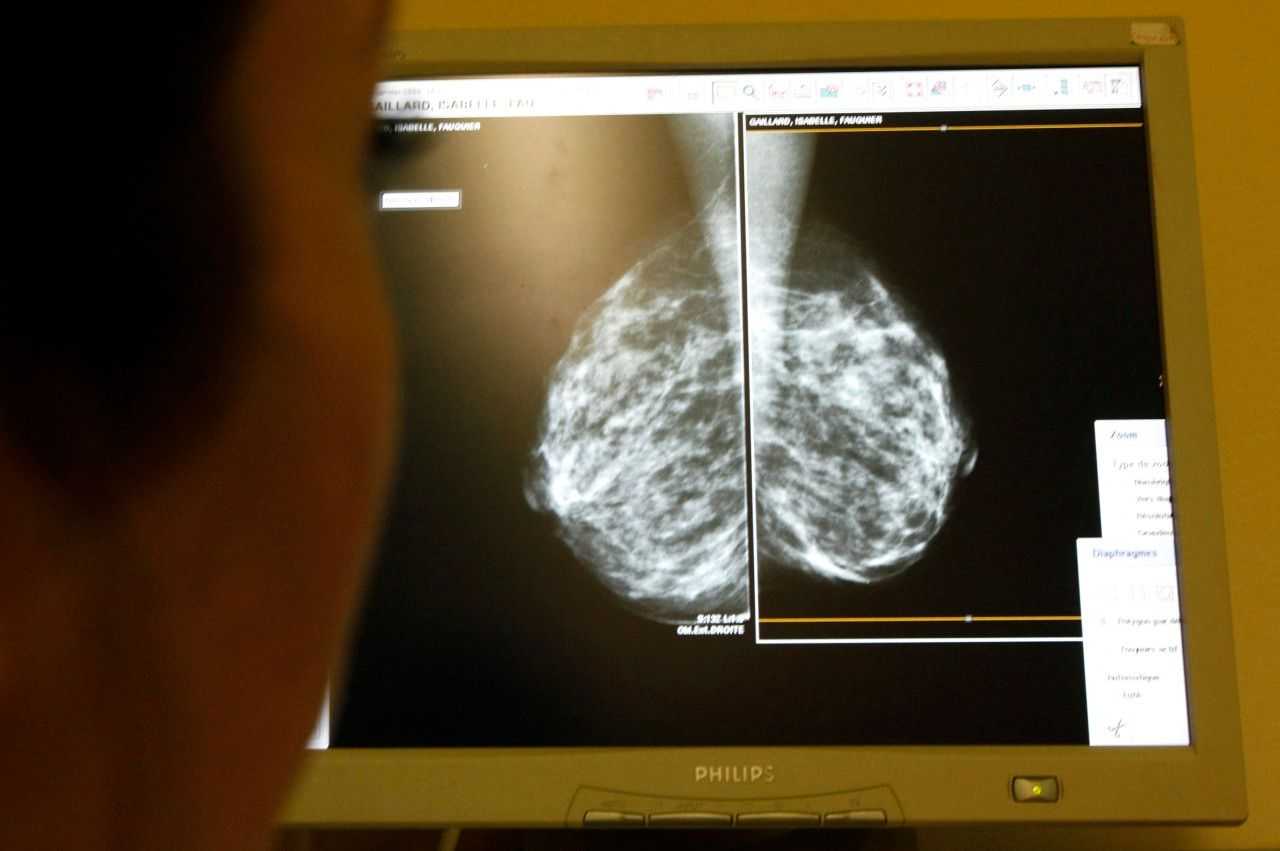
Телерисковая зона
Еще один цифровой продукт, предусмотренный к внедрению в рамках информатизации отрасли, – телемедицинские технологии, которые используются для консультирования в режиме «врач-врач» либо «врач-пациент», а также для дистанционного мониторинга за состоянием здоровья пациента. Какие здесь плюсы и минусы? Телемедицинские технологии привязаны к системе ЕГИСЗ: таким образом, каждый участник процесса распознан через единую систему идентификации и аутентификации (ЕСИА) и имеет цифровые подписи. Врач должен быть зарегистрирован в федеральном реестре медработников, а клиника – в федеральном реестре медорганизаций. Это, с одной стороны, правильно, но с другой – сложно исполнимо, особенно если речь идет о частном секторе здравоохранения. Да и пациенты в большинстве своем хотят куда более простых решений.
Кроме того, это не вопрос одного дня! Между тем регуляторика по телемедицине вступила в силу в январе 2018 года без какого-либо переходного периода. Тогда ни одна медицинская организация не была готова к этому технически, ведь требуется обеспечить защиту персональных данных пациента, передачу информации в федеральные регистры и реестры и т. д. Таким образом, о телемедицине в одночасье сделал противозаконной всю ту телемедицину, что была и довольно успешно практиковалась до 2018 года. Да и сейчас спустя 5 лет совершенно нельзя сказать, что клиники, врачи и пациенты готовы к новому формату.
Кроме технических сложностей, нормативные акты предусматривают жесткие ограничения по функционалу сервиса. Например, без очного приема врач не может поставить диагноз и назначить лечение, хотя на сегодняшний день возможности медицины и запрос пациентов шире. Уже не первый год пытаются ввести «человеческую» телемедицину на экспериментальных территориях. Это так называемые цифровые песочницы, но пока все эти задумки тоже на мели. Возможно, и потому, что многие против того, чтобы одним было можно то, что всем другим нельзя.
В итоге с 2018 года развитие телемедицины буксует, на текущий момент – это зона повышенного правового риска при одновременно больших вложениях ресурсов и высокой вероятности негатива со стороны пациентов. Телемедицина востребована и в среде врачей, однако для обращения к коллеге за помощью врачу не требуется ни ЕСИА, ни ЭЦП. Он просто возьмет телефон и позвонит. Или напишет. Теневая телемедицина еще долгие годы будет превалировать, пока условия не станут реально приемлемыми для ее участников.
Сделаем выводы из сказанного. Много и красиво говорится об информатизации отрасли, телемедицине, использовании искусственного интеллекта, но все это внедряется где-то на Олимпе, а внизу, у его подножия, ни врачи, ни клиники, ни пациенты пока не могут пользоваться всеми этими инновациями в полной мере.
К печальным выводам пришла и Счетная палата РФ в начале 2021 года. Аудиторы констатировали, что федеральная программа по созданию ЕЦК не поможет сократить временные затраты медработников, не обеспечивает высокое качество, полноту и достоверность информации о состоянии здоровья пациента, а также оптимальную маршрутизацию.
14/03/2023, 14:02
Заключение
У больных диссеминированным эстроген-позитивным РМЖ без гиперэкспрессии HER2 с прогрессированием после 3 и более линий лекарственного лечения в половине случаев эверолимус обладает не только прямым противоопухолевым эффектом (увеличение показателей выживаемости без прогрессирования), но и протективным влиянием на костную ткань вследствие ингибирования mTOR в остеокластах (уменьшение костной резорбции, индуцированной экземестаном, и снижение риска прогрессирования в костях скелета).
Это открывает перспективы применения эверолимуса в комбинации с ИА в адъювантном лечении постменопаузальных больных гормонозависимым РМЖ.
Комбинация инновационного антиmTOR-препарата эверолимуса (ингибитора передачи пролиферативного сигнала) с экземестаном (стероидным ИА) должна занять достойную нишу в лечении метастатического РЭ+ РМЖ, резистентного к эндокринотерапии. Эверолимус следует назначать тем больным мРМЖ, которые изначально не отвечают на гормонотерапию тамоксифеном и нестероидными ИА (анастрозолом или летрозолом), а также больным, у кого эффект длительного приема тамоксифена и следующего за ним нестероидного ИА уже исчерпан.
В 2012 г. была представлена доказательная база о возможности преодоления резистентности к гормонотерапии в результате применения инновационного таргетного анти-mTOR-препарата эверолимуса больными диссеминированным РЭ+ РМЖ без гиперэкспрессии HER2. Эверолимус в комбинации со стероидным ИА экземестаном – это новая опция в лечении гормоночувствительного диссеминированного РМЖ, в т. ч. с метастазами в кости, позволяющая ближе подойти к индивидуализации лечения и длительно сохранить достойное качество жизни больных.




























