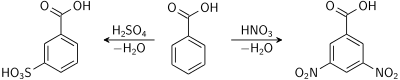
Окисление аренов
Бензол устойчив к действию даже сильных окислителей. Но гомологи бензола окисляются под действием сильных окислителей. Бензол и его гомологи горят.
3.1. Полное окисление – горение
При горении бензола и его гомологов образуются углекислый газ и вода. Реакция горения аренов сопровождается выделением большого количества теплоты.
2C6H6 + 15O2 → 12CO2 + 6H2O + Q
Уравнение сгорания аренов в общем виде:
CnH2n–6 + (3n – 3)/2 O2 → nCO2 + (n – 3)H2O + Q
При горении ароматических углеводородов в недостатке кислорода может образоваться угарный газ СО или сажа С.
Бензол и его гомологи горят на воздухе коптящим пламенем. Бензол и его гомологи образуют с воздухом и кислородом взрывоопасные смеси.
3.2. Окисление гомологов бензола
Гомологи бензола легко окисляются перманганатом и дихроматом калия в кислой или нейтральной среде при нагревании.
При этом происходит окисление всех связей у атома углерода, соседнего с бензольным кольцом, кроме связи этого атома углерода с бензольным кольцом.
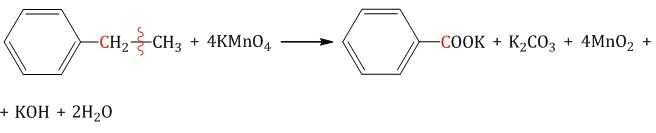
Толуол окисляется перманганатом калия в серной кислоте с образованием бензойной кислоты:
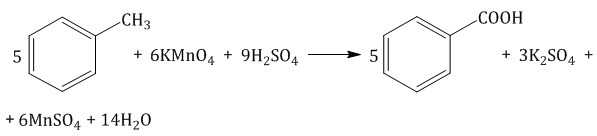
Если окисление толуола идёт в нейтральном растворе при нагревании, то образуется соль бензойной кислоты – бензоат калия:
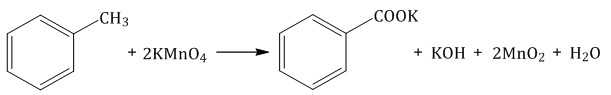
Таким образом, толуол обесцвечивает подкисленный раствор перманганата калия при нагревании.
| При окислении других гомологов бензола всегда остаётся только один атом С в виде карбоксильной группы (одной или нескольких, если заместителей несколько), а все остальные атомы углерода радикала окисляются до углекислого газа или карбоновой кислоты. |
| Например, при окислении этилбензола перманганатом калия в серной кислоте образуются бензойная кислота и углекислый газ |
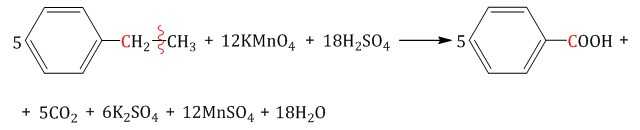
| Например, при окислении этилбензола перманганатом калия в нейтральной кислоте образуются соль бензойной кислоты и карбонат |
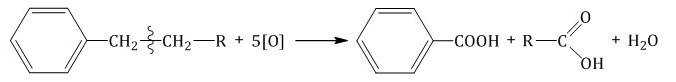
Более длинные радикалы окисляются до бензойной кислоты и карбоновой кислоты:
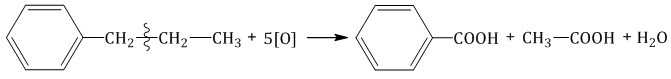
При окислении пропилбензола образуются бензойная и уксусная кислоты:
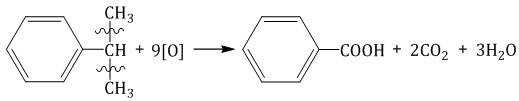
Изопропилбензол окисляется перманганатом калия в кислой среде до бензойной кислоты и углекислого газа:
Получение карбоновых кислот
Некоторые карбоновые кислоты встречаются в природе в свободном состоянии (муравьиная, уксусная, масляная, валериановая и др.). Однако, основным источником карбоновых кислот является органический синтез. Рассмотрим основные способы получения карбоновых кислот
Общие способы получения карбоновых кислот
1. Окисление первичных спиртов и альдегидов под действием различных окислителей
Окисление спиртов
В качестве окислителей применяют KMnO4 и K2Cr2O7.
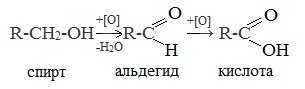
Например:
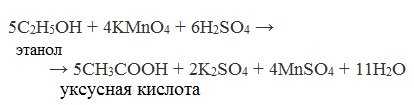
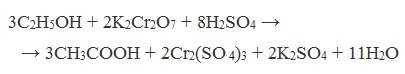
Окисление альдегидов
Для окисления альдегидов используются те же реагенты, что и для спиртов.
При окислении перманганатом калия происходит обесцвечивание фиолетово-розового раствора.
При окислении дихроматом калия — цвет меняется с оранжевого на зеленый.

А также для них характерны реакции «серебряного зеркала» и окисление гидроксидом меди (II) – качественные реакции альдегидов:
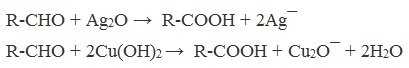
2. Гидролиз галогензамещенных углеводородов, содержащих три атома галогена у одного атома углерода
В результате реакции образуются спирты, содержащие три группы ОН у одного атома углерода. Такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:
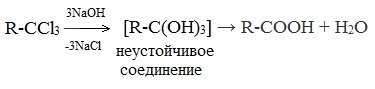
3. Получение карбоновых кислот из цианидов (нитрилов)
Этот способ позволяет наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия:
![]()
Образующийся нитрил уксусной кислоты CH3-CN (ацетонитрил, метилцианид) при нагревании гидролизуется с образованием ацетата аммония:
При подкислении раствора выделяется кислота:
![]()
4. Использование реактива Гриньяра (по схеме)
![]()
5. Гидролиз галогенангидридов кислот
С водой низшие хлорангидриды реагируют чрезвычайно энергично, образуя соответствующую карбоновую кислоту и соляную кислоту:
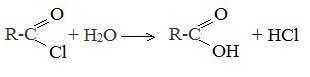
В промышленности
1. Выделяют из природных продуктов
(жиров, восков, эфирных и растительных масел)
2. Окисление алканов кислородом воздуха ( в присутствии катализаторов – солей марганца или при нагревании под давлением)
Обычно образуется смесь кислот. При окислении бутана единственным продуктом является уксусная кислота:
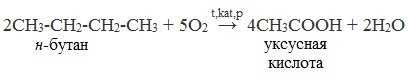
3. Окисление алкенов и алкинов
При жестком окислении алкенов кипящим раствором KMnO4 в кислой среде происходит полный разрыв двойной связи:
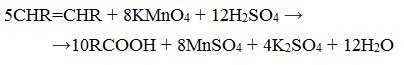
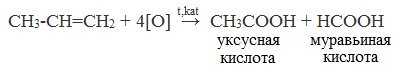
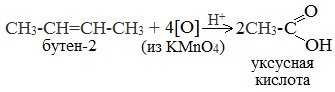
При жестком окислении (нагревание, концентрированные растворы, кислая среда) происходит расщепление углеродного скелета молекулы алкина по тройной связи и образуются карбоновые кислоты:
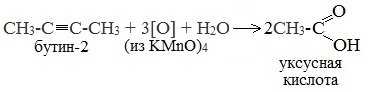
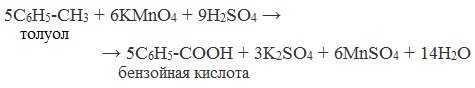
4. Окисление гомологов бензола (получение бензойной кислоты)
Для получения бензойной кислоты можно использовать окисление монозамещенных гомологов бензола кислым раствором перманганата калия:
![]()
В лаборатории
1. Гидролиз сложных эфиров
При кислотном гидролизе получают карбоновые кислоты и спирты (реакция обратная этерификации):
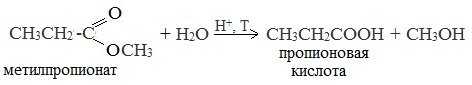
2. Из солей карбоновых кислот
![]()
3. Гидролиз ангидридов кислот
При легком нагревании с водой ангидриды образуют соответствующие карбоновые кислоты:
4. Щелочной гидролиз галоген производных карбоновых кислот
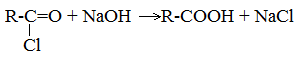
Специфические способы получения важнейших кислот
Способы получения НСООН
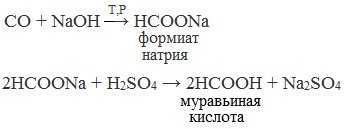
1. Взаимодействие оксида углерода (II) с гидроксидом натрия
Муравьиную кислоту получают нагреванием под давлением гидроксида натрия и оксида углерода (II) под давлением и обработкой полученного формиата натрия серной кислотой:
2. Каталитическое окисление метана
3. Декарбоксилирование щавелевой кислоты
Муравьиную кислоту можно получить при нагревании щавелевой кислоты:
Способы получения СН3СООН
Получение уксусной кислоты для химических целей
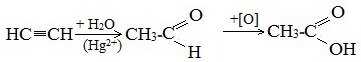
1. Синтез из ацетилена
Данный способ получения уксусной кислоты основан на окислении уксусного альдегида, который в свою очередь получают из ацетилена по реакции Кучерова (ацетилен получают из очень доступного сырья — метана):
2. Каталитическое окисление бутана
Большое значение имеет способ получения уксусной кислоты, основанный на окислении бутана кислородом воздуха:
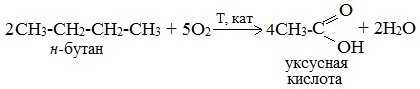
Процесс получения уксусной кислоты из метана является многостадийным (метан – ацетилен – уксусный альдегид – уксусная кислота). Ее получение окислениям будана сокращает число стадий, что дает большой экономический эффект.
3. Каталитическое карбонилирование метанола
Получение уксусной кислоты для пищевых целей
4. Уксуснокислое брожение этанола
Уксусную кислоту для пищевых целей получают уксуснокислым брожением жидкостей, содержащих спирт (вино. пиво):
![]()
Рубрики: Карбоновые кислоты Теги: Карбоновые кислоты
Опасна ли эта добавка
При накоплении Е210 в человеческом организме развиваются опасные болезни, связанные с аллергией и нарушением работы печени и почек. Вещество исследовалось на добровольцах. Те, кто получал более 1 г бензойной кислоты в сутки в течение 5 дней, жаловались на головные боли, изжогу и тошноту.
Клинические анализы доказали опасность бензойной кислоты для лиц, страдающих астмой. Описаны вредные последствия употребления Е210 для младенцев:
- повышенная
раздражительность; - боль в
области головы; - тошнота;
- рвота;
- нарушения
работы почек.
Описанные явления быстро
проходили после отмены кислоты.
Независимые источники утверждают, что Е210 может быть причиной развития рака. За основу было взято предположение, что при взаимодействии Е210 с витамином С могут образовываться канцерогенные вещество. На самом деле наличие аскорбиновой кислоты не оказывает никакого влияния на формирование канцерогенных веществ в присутствии бензойной кислоты. Для образования ракообразующих химических соединений требуется наличие высокой температуры.
Е210 смертельно опасна для кошек. Людям же рекомендуется не употреблять продукты с содержанием бензойной кислоты ежедневно. На сегодняшний день нет информации относительно того, может ли Е210 оказывать патологическое влияние на печень, поджелудочную железу или на состав крови.

Производные
- 2,3-дигидроксибензойная кислота (пирокатехиновая кислота)
- 2,4-дигидроксибензойная кислота (бета-резорциловая кислота)
- 2,5-дигидроксибензойная кислота (гентизиновая кислота)
- 2,6-дигидроксибензойная кислота (гамма-резорциловая кислота)
- 3,4-дигидроксибензойная кислота (протокатехиновая кислота)
- 3,5-дигидроксибензойная кислота (альфа-резорциловая кислота)
- 3-нитробензойная кислота
- 3,5-динитробензойная кислота
- Толуиловые кислоты
Соли
Соли бензойной кислоты называются бензоатами, например:
- Бензоат аммония
- Бензоат лития
- Бензоат натрия
- Бензоат магния
- Бензоат марганца
- Бензоат меди(II)
- Бензоат ртути(II)
- Бензоат свинца(II)
- Бензоат серебра
Как снизить мочевую кислоту?
Основа лечения гиперурикемии — излечение основного заболевания, так как избыток моч. к-ты может быть результатом врожденных генетических состояний, результатом ожирения, неправильного питания, диабета или обезвоживания.
Чтобы очистить организм от избытка кристаллов мочевой кислоты, нужно увеличить физическую активность и следовать принципам рационального питания.
Диета больных с высоким уровнем мочевой кислоты основывается в первую очередь на употреблении негазированной воды и отказе от крепкого кофе, чая и пива. Также повышают мочевую кислоту в крови напитки, содержащие фруктозу и фруктовые соки. Второй принцип — ограничение пуринов. Это диета, бедная рыбой, красным мясом, бобовыми, грибами.
Количество соли в блюдах следует ограничить, так как избыток натрия тормозит выведение мочевой кислоты с мочой.
Нужно есть больше постного мяса птицы, фруктов и зерновых. Очень хороший эффект дают настои, приготовленные из листьев березы, одуванчика и крапивы.
Назначается фармакотерапия, понижающая мочевую кислоту в крови. Наиболее распространенные лекарства: фебуксостат и аллопуринол. Помимо приема лекарств нужно бросить курить.
Точные рекомендации всегда должны быть согласованы с лечащим врачом (например, урологом, ревматологом), который также принимает решение о необходимости возможной фармакотерапии.
Биологическое действие и влияние на здоровье человека
Бензойная кислота в свободном виде и виде сложных эфиров встречается в составе многих растений и животных. Значительное количество бензойной кислоты находится в ягодах (около 0,05 %). Зрелые плоды некоторых видов вакциниума содержат большое количество свободной бензойной кислоты. Например, в бруснике — до 0,20 % в спелых ягодах, и в клюкве — до 0,063 %. Бензойная кислота также образуется в яблоках после заражения грибком Nectria galligena. Среди животных, бензойная кислота обнаружена в основном во всеядных или фитофагных видах, например, во внутренних органах и мускулах тундряной куропатки (Lagopus muta), также как и в выделениях самцов овцебыка или азиатского слона.
Бензойная смола содержит до 20 % бензойной кислоты и 40 % бензойных эфиров.
Бензойная кислота присутствует, как часть гиппуровой кислоты (N-бензоилглицин) в моче млекопитающих, особенно травоядных животных. Бензойная кислота хорошо всасывается, через коэнзим А связывается с аминокислотой глицином в гиппуровую кислоту и в таком виде выводится через почки. Человек выделяет около 0,44 г/л гиппуровой кислоты в день в моче и больше, если находится в контакте с толуолом или бензойной кислотой. Для человека считается безопасным потребление 5 мг/кг массы тела в день. Кошки имеют гораздо более низкую толерантность к бензойной кислоте, чем мыши и крысы. Летальная доза для кошек — 300 мг/кг массы тела. Оральная ЛД50 для крыс 3040 мг/кг, для мышей 1940—2260 мг/кг.
Бензольное кольцо
Электрофильное ароматическое присоединение происходит по 3-му положению из-за электроноакцепторных свойств карбоксильной группы. Второе замещение происходит сложнее (правая часть) благодаря деактивации нитрогруппой. Наоборот, при введении электронодонорного заместителя (например, алкила), второе замещение происходит легче.
Карбоксильная группа
Все реакции, характерные для карбоксильной группы, возможны с бензойной кислотой:
- Эфиры бензойной кислоты — продукты кислотнокатализируемой реакции со спиртами
- Амиды бензойной кислоты легко доступны, используя для их синтеза активированные производные(такие как бензоилхлорид), или сочетающие реагенты используемые в пептидном синтезе такие как ДЦГК и ДМАП.
- Более активный бензойный ангидрид образуется при дегидратации уксусным ангидридом или оксидом фосфора
- Высокоактивные галогенангидриды легко получаются действием хлоридом фосфора(V) или тионилхлорида
- Ортоэфиры могут быть получены в сухих условиях реакцией бензонитрила в кислой среде со спиртами
- Восстановление до бензальдегида или бензилового спирта возможно при использовании LiAlH4 или борогидрида натрия
- Декарбоксилирование серебряной соли может быть проведено при нагревании, бензойная кислота может быть декарбоксилирована при нагревании с сухими щёлочами или гидроксидом кальция.
- Бензойная кислота образует соли
Химические свойства
Данное вещество – одноосновная карбоновая кислота ароматического ряда. Рацемическая формула Бензойной кислоты: C7H6O2. Структурная формула: C6H5COOH. Впервые была синтезирована еще в 16 веке из росного ладана, бензойной смолы, откуда и получила свое название. Это белые мелкие кристаллы, которые плохо растворяются в воде, хорошо растворимы в хлороформе, этаноле и диэтиловом эфире. Молекулярная масса вещества = 122,1 грамм на моль.
Химические свойства Бензойной кислоты. Вещество проявляет слабые кислотные свойства, достаточно легко возгоняется и перегоняется с помощью водяного пара. Вступает во все реакции, характерные для карбоксильной группы. Реакция нитрования (HNO3) протекает сложнее, чем электрофильное ароматическое присоединение в 3-ем положении. При введении заместителя, например, алкила, легче происходит замещение во второй позиции. Химическое соединение образует эфиры, амиды, бензойный ангидрид, галогенангидриды, ортоэфиры, соли.
Качественная реакция на Бензойную кислоту. Чтобы установить подлинность вещества проводят реакцию с хлоридом железа 3, FeCl3, в результате образуется плохо растворимый в воде комплексный основной бензоат железа 3, обладающий характерной желто-розовой окраской.
Получение из толуола. Чтобы Бензойную кислоту получить из толуола, необходимо воздействовать на средство сильным окислителем, например, MnO2 в присутствии катализатора – серной к-ты. В результате образуется вода и ионы Mn2+. Также толуол можно окислить перманганатом калия. Для того, чтобы провести реакцию получения Бензойной Кислоты из бензола сначала необходимо получить толуол: бензол + CH3Cl, в присутствии хлорида алюминия = толуол + соляная кислота. Также при получении вещества используют реакции гидролиза бензамида и бензонитрила; реакцию Канниццаро или реакцию Гриньяра (карбоксилирование фенилмагнийбромида).
- для калибровки калориметров, используется в качестве теплового стандарта;
- сырье для получения бензоилхлорида, фенола, бензоатных пластификаторов;
- в качестве консерванта, в чистом виде или в виде натриевых, кальциевых и калиевых солей, код E210, E212, E211, E213;
- при некоторых кожных заболеваниях и в качестве отхаркивающего средства (натриевая соль);
- в парфюмерной промышленности используют эфиры кислоты;
- нитро- и хлорбензойная кислота используется при синтезе красителей.
Статья составлена с использованием следующих материалов:
Апасов И.В., Фоменко Г.К. Эффективность препаратов для повышения сохранности сахарной свеклы при хранении. Журнал «Сахар» №4, 2011 год, с. 37-39
2.
Бердников А.С., Сапронов Н.М. Хранение сахарной свеклы современных гибридов с применением полифункциональных препаратов. Материалы всероссийской научно-практической конференции «Аграрная наука – сельскому хозяйству» 27-28 января 2009 г. Курская государственная сельско-хозяйственная академия им. И.И. Иванова. – Курск, 2009. ч.4. с 39-41
3.
Буклет «Кагатник», ЗАО «Щелково Агрохим», Россия
4.
Государственный каталог пестицидов и агрохимикатов, разрешенных к применению на территории Российской Федерации, 2013 год. Министерство сельского хозяйства Российской Федерации (Минсельхоз России)
5.
Государственный каталог пестицидов и агрохимикатов, разрешенных к применению на территории Российской Федерации, 2022 год. Министерство сельского хозяйства Российской Федерации (Минсельхоз России)
6.Кнунянц И.Л. Химическая энциклопедия: В 5 т./Ред. кол. Кнунянц И.Л. (гл. ред.) и др. – М.: Советская энциклопедия. 1988.
Свернуть
Список всех источников
Структура бензойной кислоты
На верхнем изображении структура бензойной кислоты представлена в виде стержня и сферы. Если подсчитать количество черных сфер, то будет проверено, что их шесть, то есть шесть атомов углерода; две красные сферы соответствуют двум атомам кислорода карбоксильной группы -COOH; и, наконец, белые сферы являются атомами водорода.
Как видно, ароматическое кольцо слева, ароматичность которого показана пунктирными линиями в центре кольца. А справа группа -COOH, ответственная за кислотные свойства этого соединения.
Молекулярно, С6H5COOH имеет плоскую структуру, потому что все его атомы (кроме водорода) имеют sp-гибридизацию2.
С другой стороны, группа -COOH, очень полярная, позволяет постоянному диполю существовать в структуре; диполь, который можно наблюдать с первого взгляда, если доступна его карта электростатического потенциала.
Этот факт как следствие того, что C6H5COOH может взаимодействовать с самим собой диполь-дипольными силами; в частности, со специальными водородными мостиками.
Если наблюдается группа -COOH, будет обнаружено, что кислород C = O может принимать водородную связь; в то время как кислород O-H дарит им.
Хрустальные и водородные мосты
Бензойная кислота может образовывать две водородные связи: она получает и принимает одну одновременно. Следовательно, он образует димеры; то есть его молекула «связана» с другим.
Являются ли эти пары или димеры, C6H5COOH-HOOCC6H5, структурная основа, которая определяет твердое тело в результате его упорядочения в пространстве.
Эти димеры образуют плоскость молекул, которые, благодаря своим сильным и направленным взаимодействиям, способны установить упорядоченную структуру в твердом теле. Ароматические кольца также участвуют в этой договоренности через взаимодействия дисперсионных сил.
В результате молекулы образуют моноклинный кристалл, точные структурные характеристики которого можно изучить с помощью инструментальных методов, таких как дифракция рентгеновских лучей..
Тогда пара плоских молекул может быть размещена в пространстве преимущественно водородными связями, чтобы вызвать появление этих белых и кристаллических игл..
Цена, где купить
Образование: Окончила Ровенский государственный базовый медицинский колледж по специальности «Фармация». Окончила Винницкий государственный медицинский университет им. М.И.Пирогова и интернатуру на его базе.
Опыт работы: С 2003 по 2013 г. – работала на должностях провизора и заведующего аптечным киоском. Награждена грамотами и знаками отличия за многолетний и добросовестный труд. Статьи на медицинскую тематику публиковались в местных изданиях (газеты) и на различных Интернет-порталах.
- Свежие записи
- Укладываем художественный паркет самостоятельно
- Как лучше всего защитить стены из газоблока от разрушения в первую зиму после строительства дома
- Арболит, он же — опилкобетон
- Особенности звукоизоляции помещений
- Глина с опилками – самый лучший и дешевый способ утепления бетонных стен дома
- Правообладателям
- Политика конфиденциальности
Строение бензойной кислоты
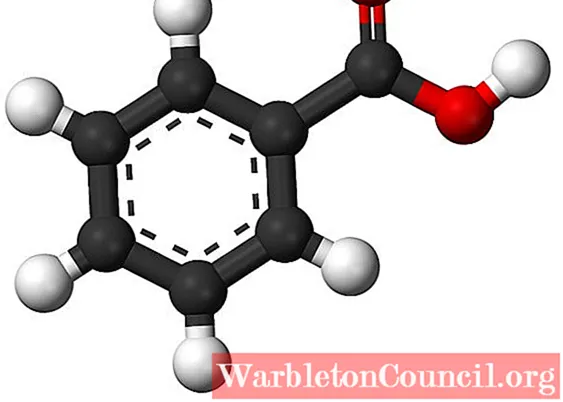
Верхнее изображение представляет структуру бензойной кислоты в виде стержня и сферы. Если подсчитать количество черных сфер, будет подтверждено, что их шесть, то есть шесть атомов углерода; две красные сферы соответствуют двум атомам кислорода карбоксильной группы –COOH; и, наконец, белые сферы — это атомы водорода.
Как видно, слева находится ароматическое кольцо, ароматичность которого иллюстрируется пунктирными линиями в центре кольца. А с правой стороны — группа –COOH, отвечающая за кислотные свойства этого соединения.
Молекулярно C6ЧАС5COOH имеет плоскую структуру из-за того, что все его атомы (кроме атомов водорода) имеют sp-гибридизацию.2.
С другой стороны, высокополярная группа –COOH позволяет постоянному диполю существовать в структуре; диполь, который можно было бы наблюдать с первого взгляда, если бы была доступна его карта электростатического потенциала.
Как следствие этого факта, C6ЧАС5COOH может взаимодействовать с самим собой посредством диполь-дипольных сил; в частности, со специальными водородными связями.
Если вы посмотрите на группу –COOH, вы обнаружите, что кислород в C = O может принимать водородную связь; в то время как кислород из OH отдает их.
Чем пахнет бензоин
Аромат бензоина трудно описать, он одновременно эфемерен и вязок, приятен и необычен, но спутать его с каким-то другим запахом просто невозможно. Аромат коррелируется составом и зависит от географического расположения плантаций дерева.
Тайская и китайская смола – более качественна, по мнению специалистов. В ней больше сладости, она напоминает медово-сливочную ваниль, в которой гармонично сочетаются запахи пряностей, ванили, смолы, бальзамических и сливочных нот.
Аромат яркий, насыщенный, сложный. В парфюмерии бензоин идеален для создания восточных композиций. Только так можно предать восточную ночь, например, темнота которой, кажется, режется ножом, настолько она насыщена.
Вещество испокон веков используют как афродизиак. В Средневековье его называли «молоком девственницы», в его состав включали лаванду и этанол. О том, что бензоин повышает потенцию и восстанавливает репродуктивную функцию, хорошо знают и сегодня.
В древности камедь раскуривали в храмах, чтобы отогнать злых духов. Объясняется такое свойство вещества просто – это антисептик, регенерант, быстро заживляющий раны. Вenzoin обладает бодрящими свойствами, тонизирует, помогает купировать депрессии.
Структурная изомерия
Для предельных карбоновых кислот характерна структурная изомерия – изомерия углеродного скелета и межклассовая изомерия.
Структурные изомеры – это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета характерна для карбоновых кислот, которые содержат не менее четырех атомов углерода.
| Например. Формуле С4Н8О2 соответствуют бутановая и 2-метилпропановая кислота |
| Бутановая (масляная) кислота | Изомасляная (2-метилпропановая) кислота |
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Карбоновые кислоты изомерны сложным эфирам. Общая формула и предельных одноосновных карбоновых кислот, и сложных эфиров — CnH2nО2.
| Например. Межклассовые изомеры с общей формулой С2Н4О2: уксусная кислота СН3–CОOH и метилформиат H–COOCH3 |
| Уксусная кислота | Метиловый эфир муравьиной кислоты |
| СН3–CОOH | HCOOCH3 |
Общую формулу СnH2nO2 могут также иметь многие другие полифункциональные соединения, например: альдегидоспирты, непредельные диолы, циклические простые диэфиры и т.п.
Химические свойства карбоновых кислот
.
Для карбоновых кислот характерны следующие свойства:
|
1. Кислотные свойства
| Кислотные свойства карбоновых кислот возникают из-за смещения электронной плотности к карбонильному атому кислорода и вызванной этим дополнительной (по сравнению со спиртами и фенолами) поляризацией связи О–Н. |
|
Карбоновые кислоты – кислоты средней силы.
В водном растворе карбоновые кислоты частично диссоциируют на ионы: R–COOH ⇆ R-COO– + H+ |
1.1. Взаимодействие с основаниями
Карбоновые кислоты реагируют с большинством оснований. При взаимодействии карбоновых кислот с основаниями образуются соли карбоновых кислот и вода.
CH3COOH + NaOH = CH3COONa + H2O
Карбоновые кислоты реагируют с щелочами, амфотерными гидроксидами, водным раствором аммиака и нерастворимыми основаниями.
| Например, уксусная кислота растворяет осадок гидроксида меди (II) |
| Например, уксусная кислота реагирует с водным раствором аммиака с образованием ацетата аммония |
CH3COOH + NH3 = CH3COONH4
1.2. Взаимодействие с металлами
Карбоновые кислоты реагируют с активными металлами. При взаимодействии карбоновых кислот с металлами образуются соли карбоновых кислот и водород.
| Например, уксусная кислота взаимодействует с кальцием с образованием ацетата кальция и водорода. |
1.3. Взаимодействие с основными оксидами
Карбоновые кислоты реагируют с основными оксидами с образованием солей карбоновых кислот и воды.
| Например, уксусная кислота взаимодействует с оксидом бария с образованием ацетата бария и воды. |
| Например, уксусная кислота реагирует с оксидом меди (II) |
2СН3СООН + CuO = H2О + ( CH3COO)2 Cu
1.4. Взаимодействие с с солями более слабых и летучих (или нерастворимых) кислот
Карбоновые кислоты реагируют с солями более слабых, нерастворимых и летучих кислот.
| Например, уксусная кислота растворяет карбонат кальция |
| Качественная реакция на карбоновые кислоты: взаимодействие с содой (гидрокарбонатом натрия) или другими гидрокарбонатами. В результате наблюдается выделение углекислого газа |
Опасные ешки таблица. Опасные пищевые добавки и их влияние на организм человека
Ниже приведён список наиболее распространённых пищевых добавок, составляющих опасность для здоровья человека. Они достаточно широко используются в пищевой промышленности, несмотря на причиняемый ими вред.
Жёлто-зелёный хинолин (Е104) является красителем. Его добавляют в сладости, жевательную резинку, газированные напитки, бакалейные продукты, копчёную рыбу. Он может вызывать сильные аллергические реакции, заболевания желудочно-кишечного тракта. Оказывает негативное влияние на здоровье детей.
Бензойная кислота и её производные (Е210–213) наносят большой вред здоровью человека, особенно у детей. Они вызывают сильные аллергические реакции и развитие раковых заболеваний, нервное возбуждение, негативно влияют на дыхательную систему и интеллект человека. Список продуктов, в которые входят эти пищевые добавки, огромен. Вот некоторые из них: чипсы, кетчуп, овощные и мясные консервы, газированные напитки, сок. Тем не менее, эти вещества не запрещены во многих странах.
Сульфиты (Е221-228) — это группа пищевых добавок, которые ещё плохо изучены и считаются опасными для здоровья человека. Они являются консервантами и добавляются во фруктовые и овощные консервы, картофельные пюре быстрого приготовления, томатные пасты, крахмал, вино. Ими обрабатываются сухофрукты и проводится дезинфекция тар. Эти вещества способны вызывать сильные аллергические реакции, провоцировать приступы бронхиальной астмы, раздражая дыхательные пути, и заболевания ЖКТ. При нарушении технологии приготовления продуктов они могут привести к смерти.
Уротропин (Е239) увеличивает сроки хранения сыров и консервированной икры. Является опасным для здоровья человека из-за сильного канцерогенного действия. Он также является мощным аллергеном и вызывает различные заболевания кожи.
Нитриты и нитраты (Е250-252). Эти пищевые добавки добавляют в колбасные изделия для придания им насыщенного розового цвета. К тому же они способны защищать продукты от окисления и воздействия микробных агентов. Несмотря на такие положительные качества, эти вещества очень опасны для здоровья человека, потому что оказывают мощное канцерогенное действие, провоцируя развитие рака лёгких и кишечника. На них часто бывают аллергические реакции вплоть до удушья. Также они оказывают влияние на сердечно-сосудистую систему, то сужая, то расширяя сосуды, вызывая тем самым резкие скачки артериального давления. Влияют нитраты и на нервную систему. Проявляется это головными болями, нарушением координацией, судорогами.
Пропионаты (Е280-283) служат консервантами. Их добавляют в молочную продукцию, хлебобулочные изделия, различные соусы. Они оказывают негативное влияние на сосуды головного, вызывая их спазм. При большом употреблении этих химикатов может появляться мигрень. Их не рекомендуют давать детям.
Углекислый газ (Е290) является одним из основных компонентов газированных напитков. Он способен вымывать кальций, что очень вредно для растущего организма. Может провоцировать обострение гастрита и язвенной болезни желудка, отрыжки и метеоризм.
Хлористый аммоний (Е510) служит улучшителем теста. Его добавляют в дрожжи, хлеб, хлебобулочные изделия, диетическое питание и муку. Оказывает сильное негативное влияние на желудочно-кишечный тракт, особенно на печень и кишечник.
Глутамат натрия (Е621) является одной самых известных пищевых добавок. Он входит в группу усилителей вкуса. Нашумевшая его опасность немного преувеличена. На самом деле, глутамат натрия является компонентом бобовых, водорослей, соевого соуса. В небольших количествах он совершенно безвреден для организма человека. Но при систематическом употреблении большого количества продуктов, содержащих его (чипсы, приправы, соусы, полуфабрикаты), происходит накопление и отложение в различных органах солей натрия. В результате этого могут развиваться болезни: снижение остроты зрения, тахикардия, общая слабость, выраженные головные боли, нервное возбуждение, аллергии (зуд кожных покровов и гиперемия лица).Это далеко не полный перечень. В него включены только наиболее опасные и часто используемые пищевые добавки. На самом же деле их существует намного больше.
Химические свойства
Бензойная кислота проявляет все свойства карбоновых кислот: образование эфиров при взаимодействии со спиртами, образования амидов и тому подобное.
Бензойная кислота устойчива к действию многих окислителей: воздух, перманганат, гипохлоритов. Однако, при нагревании свыше 220 ° C она взаимодействует с солями меди (II), образуя фенол и его производные. В результате взаимодействия кислоты с аммиаком образуется анилин.
Нагрев бензойную кислоту до 370 ° C в присутствии катализатора (медный или кадмиевый порошки), происходит декарбоксилирование, что ведет к бензола на незначительных количеств фенола.
При участии катализатора оксида циркония бензойную кислота может гидруватися к бензальдегида с количественным выходом. А гидрирования в присутствии благородных металлов ведет к образованию циклогексанкарбоновои кислоты (гексагидробензойнои).
Хлорирование соединения дает продуктом преимущественно 3-хлоробензойну кислоту. Нитрования и сульфирования происходит аналогично по третьему положением.