Интерферон лейкоцитарный человеческий
Если инфекция преодолевает вышеуказанные общие физиологические и гуморальные факторы, ей удается проникнуть в чувствительную клетку. После этого запускается процесс внутриклеточного развития вируса, но в некоторых случаях проникновение инфекции не всегда сопровождается внутриклеточным поражением. Морфологически клетка не меняется, никаких деструктивных процессов в ней не происходит, поэтому в дальнейшем она становится устойчивой к штаммам этого вируса.
Противовирусный иммунитет, выработанный в результате вирусной интерференции, считается самым сильным. В его материальной основе лежит продуцирование особого вещества – интерферона. Этот белок образуется как ответная реакция на проникновение патогена в клетку. Интерферон обладает противовирусными, антипролиферативными и иммуномодулирующими свойствами и теряет свою активность, но не погибает при низких температурах. Разрушить его можно воздействием ультрафиолета и высоких температур (выше 60 °С).
В крови интерферон появляется спустя 1-2 часа после проникновения вируса и максимальной концентрации достигает через 4-8 ч. Белок возникает как реакция в ответ не только на проникновение вирусов, но и бактерий, продуктов их жизнедеятельности, являясь основным элементом противовирусного иммунитета.
Интерферон присутствует в крови, моче, спинномозговой жидкости, секрете носоглотки, в почках, легких и в соединительной ткани организма. Его вырабатывают практически все клетки, но в большей степени этот белок продуцируется селезенкой и лейкоцитами. Принцип действия интерферона состоит в подавлении функции размножения вируса при полном сохранении жизнедеятельности клетки.
Слайд 5Гуморальные факторы. ИнтерфероныИнтерфероны – гликопептиды, вырабатывающиеся и аккумулирующиеся во всех ядросодержащих
клетках крови и эпителиальных клетках слизистых оболочек являются цитокинами с широким спектром биологических активностей:противовирусное действие, ингибирование гемопоэза; модуляция иммунного и воспалительного ответов, регуляция пролиферации и дифференцировки клеток и т.д. При вирусной инфекции клетки синтезируют интерферон и секретируют его в межклеточное пространство, где он связывается со специфическими рецепторами соседних незараженных клеток.– Связанный интерферон оказывает противовирусное действие. – Конечный результат состоит из образования барьера из устойчивых к вирусу неинфицированных клеток вокруг очага инфекции, чтобы ограничить ее распространение.

Препараты с действием, направленным на элиминацию вируса
В наши дни существует большое количество групп препаратов, предназначенных для выведения и уничтожения вирусов . Все их можно условно разделить на две группы:
- Аналоги нуклеозидов — препараты-блокаторы синтеза ДНК и РНК. Как мы уже писали выше, ядро вируса состоит из ДНК и РНК. Средства данной группы воздействуют именно на нее — под действием веществ, содержащихся в блокаторах, синтез ДНК прекращается, и распространение вируса останавливается
- Ингибиторы активных белков вируса. Эти средства воздействуют на капсид — белковую оболочку вируса. Действие препаратов приводит к невозможности репликации вируса, его проникновения в здоровые клетки или выхода из инфицированной клетки.
Факторы, прогнозирующие тяжесть заболевания
Остается неясным, почему у некоторых инфицированных людей симптомы отсутствуют, тогда как у других наблюдается тяжелый COVID-19. Однако с тяжелым COVID-19 связаны:
- Нарушение врожденных иммунных ответов интерферона I типа.
- Цитомегаловирус (CMV) и вирус простого герпеса 1 (HSV-1).
- Мужской пол. Мужчины, госпитализированные с COVID-19, имеют более сильный ответ антител и повышенную тяжесть заболевания по сравнению с женщинами.
- Возраст > 65 лет. У пожилых людей во время острой инфекции SARS-CoV-2 чаще наблюдались нерегулируемые реакции приобретенного иммунитета, чем у более молодых людей.
- Состав кишечного микробиома. Американские исследователи показали, что увеличение количества кишечных бактерий Enterococcus faecalis – главный предиктор тяжелого COVID-19.
Возможность выявления прогностических факторов будет увеличена за счет включения бессимптомных лиц, инфицированных SARS-CoV-2.
Слайд 14Нормальные киллеры (NK-
клетки
Механизм дифференциации нормальных и вирусинфицированных клеток связан с двумя рецепторами, экспрессирующимися на мембране НК-клеток. Один из них — NKR-P1 — является основным в реализации киллерной функции данных клеток.
В результате взаимодействия этого рецептора с соответствующим лигандом на любой из возможных клеток создаются условия для реализации киллерного действия. При этом действие НК-клеток против собственных нативных клеток блокируется вторым рецептором — Ly49 , способным контактировать с молекулами I класса МНС , что предотвращает лизис нативных собственных клеток.Инфицированные вирусом клетки становятся чувствительными к НК одним из двух способов.некоторые вирусы подавляют белковый синтез в клетках хозяина, в результате селективно блокируется синтез молекул I класса МНС, индуцированный интерфероном, и Ly49-рецептор будет не в состоянии предотвращать киллерную активность НК-клеток.некоторые вирусы препятствуют экспрессии молекул I класса МНС, что также делает вирусинфицированные клетки объектом киллерного действия НК-клеток.

Перекрестно-реактивные T- клетки и антитела
На ответы приобретенного иммунитета могут влиять предыдущие встречи с вирусами. Например, ТRM-клетки, находящиеся в легких, могут распознавать внутренние структурные белки вирусов гриппа и впоследствии снижать тяжесть заражения новыми штаммами вируса гриппа. Т-клетки, реактивные к белкам SARS-CoV-2, были обнаружены у лиц, ранее инфицированных SARS-CoV, и у здоровых людей, не подвергавшихся воздействию этих коронавирусов. Эти результаты показывают, что Т-клетки памяти генерируются при заражении другими коронавирусами человека (HCoV), включая простудные коронавирусы. Было обнаружено, что антитела IgG пациентов с COVID-19 сильно реагируют на белки вируса гепатита C. Напротив, SARS-CoV-2-реактивные антитела, специфические для белков HCoV, были обнаружены в сыворотках людей, не болевших COVID-19, – это могут быть широко нейтрализующие антитела.
Пока неясно, могут ли уже существующие SARS-CoV-2-реактивные Т- и В-клетки способствовать улучшению исходов заболевания. Если они улучшают исход заболевания, то может быть желательно увеличить такие популяции Т- и В-клеток с помощью вакцинации.
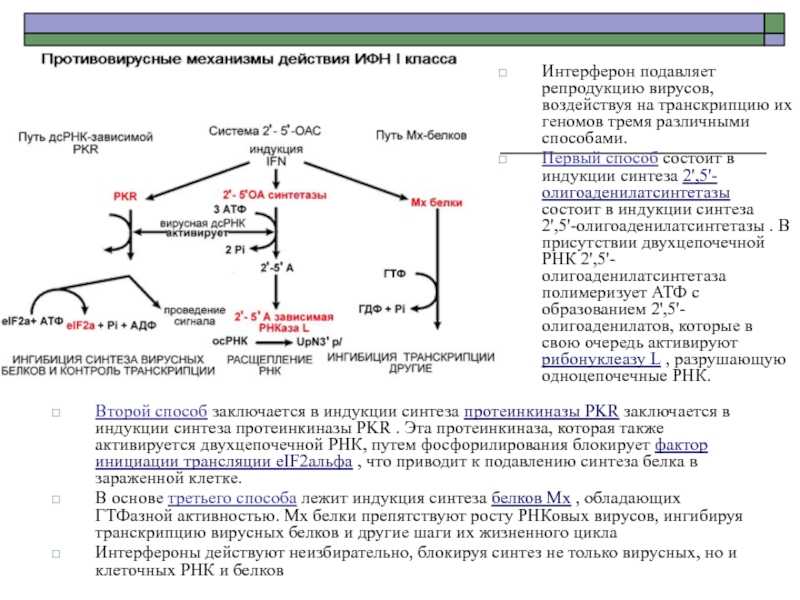
Слайд 9Второй способ заключается в индукции синтеза протеинкиназы PKR заключается в индукции
синтеза протеинкиназы PKR . Эта протеинкиназа, которая также активируется двухцепочечной РНК, путем фосфорилирования блокирует фактор инициации трансляции eIF2альфа , что приводит к подавлению синтеза белка в зараженной клетке.В основе третьего способа лежит индукция синтеза белков Мх , обладающих ГТФазной активностью. Mx белки препятствуют росту РНКовых вирусов, ингибируя транскрипцию вирусных белков и другие шаги их жизненного цикла Интерфероны действуют неизбирательно, блокируя синтез не только вирусных, но и клеточных РНК и белков
Интерферон подавляет репродукцию вирусов, воздействуя на транскрипцию их геномов тремя различными способами. Первый способ состоит в индукции синтеза 2′,5′-олигоаденилатсинтетазы состоит в индукции синтеза 2′,5′-олигоаденилатсинтетазы . В присутствии двухцепочечной РНК 2′,5′-олигоаденилатсинтетаза полимеризует АТФ с образованием 2′,5′-олигоаденилатов, которые в свою очередь активируют рибонуклеазу L , разрушающую одноцепочечные РНК.
Особенности противовирусного иммунитета
4. Особенности противовирусного иммунитета
Противовирусный иммунитет начинается со стадии презентации вирусного антигена Т-хелперами.
Сильными антигенпрезентирующими свойствами при вирусных инфекциях обладают дендритные клетки, а при простом герпесе и ретровирусных инфекциях – клетки Лангерганса.
Иммунитет направлен на нейтрализацию и удаление из организма вируса, его антигенов и зараженных вирусом клеток. Антитела, образующиеся при вирусных инфекциях, действуют непосредственно на вирус или на клетки, инфицированные им. В этой связи выделяют две основные формы участия антител в развитии противовирусного иммунитета:
1) нейтрализацию вируса антителами; это препятствует рецепции вируса клеткой и проникновению его внутрь. Опсонизация вируса с помощью антител способствует его фагоцитозу;
2) иммунный лизис инфицированных вирусом клеток с участием антител. При действии антител на антигены, экспрессированные на поверхности инфицированной клетки, к этому комплексу присоединяется комплемент с последующей его активацией, что и обуславливает индукцию комплементзависимой цитотоксичности и гибель инфицированной вирусом клетки.
Недостаточная концентрация антител может усиливать репродукцию вируса. Иногда антитела могут защищать вирус от действия протеолитических ферментов клетки, что при сохранении жизнеспособности вируса приводит к усилению его репликации.
Вируснейтрализующие антитела действуют непосредственно на вирус лишь в том случае, когда он, разрушив одну клетку, распространяется на другую.
Когда вирусы переходят из клетки в клетку по цитоплазматическим мостикам, не контактируя с циркулирующими антителами, то основную роль в становлении иммунитета играют клеточные механизмы, связанные прежде всего с действием специфических цитотоксических Т-лимфоцитов, Т-эффекторов и макрофагов. Цитотоксические Т-лимфоциты непосредственно контактируют с клеткой-мишенью, повышая ее проницаемость и вызывая осмотическое набухание, разрыв мембраны и выход содержимого в окружающую среду.
Механизм цитотоксического эффекта связан с активацией мембранных ферментных систем в зоне прилипания клеток, образованием цитоплазматических мостиков между клетками и действием лимфотоксина. Специфические Т-киллеры появляются уже через 1–3 дня после заражения организма вирусом, их активность достигает максимума через неделю, а затем медленно понижается.
Одним из факторов противовирусного иммунитета является интерферон. Он образуется в местах размножения вируса и вызывает специфическое торможение транскрипции вирусного генома и подавление трансляции вирусной мРНК, что препятствует накоплению вируса в клетке-мишени.
Стойкость противовирусного иммунитета вариабельна. При ряде инфекций (ветряной оспе, паротите, кори, краснухе) иммунитет достаточно стойкий, а повторные заболевания встречаются крайне редко. Менее стойкий иммунитет развивается при инфекциях дыхательных путей (гриппе) и кишечного тракта.
Данный текст является ознакомительным фрагментом.
источник
Особенности противовирусного иммунитета

Врожденный иммунитет – это первичная защитная реакция организма, которая срабатывает незамедлительно при вторжении вируса. Он обеспечивает быстрый, но непродолжительный ответ на инфекцию. В состав врожденного иммунитета входят физические барьеры (кожа, слизистые оболочки), клетки фагоцитарной системы (нейтрофилы, макрофаги), комлементарная система, натуральные киллеры и др.
Адаптивный иммунитет – это специализированная защитная реакция, которая развивается в ответ на конкретный вирус. Он требует некоторого времени для активации, но обеспечивает более продолжительный и эффективный ответ на инфекцию. Адаптивный иммунитет осуществляется с помощью специфических клеток (лимфоциты) и антител.
В процессе противовирусного иммунитета организм выполняет несколько основных функций:
ФункцияОписание
| Распознавание вирусов | Иммунитет распознает вирусы с помощью специальных рецепторов, которые связываются с вирусными антигенами. |
| Уничтожение вирусов | Иммунные клетки, такие как нейтрофилы и натуральные киллеры, атакуют и уничтожают вирусы. |
| Формирование иммунологической памяти | Адаптивный иммунитет запоминает вирусы, с которыми он ранее сталкивался, и при повторном заражении быстро и эффективно реагирует на них. |
| Производство антител | Антитела являются специфическими белками, которые связываются с вирусами и помогают их уничтожить. |
Особенности противовирусного иммунитета различаются в зависимости от типа вируса и индивидуальных особенностей организма. Некоторые вирусы могут эвадировать от иммунного ответа, другие вызывают сильные иммунные реакции, приводящие к воспалению и тканевым повреждениям.
Понимание особенностей противовирусного иммунитета позволяет разрабатывать эффективные методы профилактики и лечения вирусных инфекций.
Механизм распознавания и устранения вируса
Как Т-клеточное распознавание вирусных пептидов, так и В-клеточное распознавание вирусных белков начинаются в лимфоидных тканях, где дендритные клетки представляют пептиды Т-клеткам, а В-клетки отбирают вирусные белки. Вместе они инициируют развитие эффекторных клеток для устранения вируса.
Величина ответов Т- и В-клеток определяется:
- патогенностью вируса;
- степенью воспаления;
- частотой вирус-специфических Т- и В-клеток;
- кинетикой репликации вируса.
CD8+ Т-клетки – T-киллеры – дифференцируются в эффекторные клетки, которые ограничивают репликацию вируса, уничтожая инфицированные клетки. CD4+ Т-клетки – T-хелперы – дифференцируются в эффекторные клетки, которые подавляют репликацию вируса и поддерживают CD8+ Т-клетки, а также дифференцировку В-клеток. Как CD8+, так и CD4+ Т-клетки продуцируют противовирусный и иммуномодулирующий пептид интерферон гамма. Чтобы запустить противовирусную реакцию, эффекторные Т-клетки могут проникать в кровоток и перемещаться к очагам инфекции.
CD4+ Т-клетки также дифференцируются в фолликулярные Т-хелперы (ТFH), которые необходимы для развития продуцирующих антитела В-клеток и поддерживают развитие В-клеток памяти. ТFH имеют решающее значение для формирования зародышевых центров в фолликулах периферических лимфоидных органов.
Антитела могут нейтрализовать вирусы, предотвращая проникновение в клетки или способствуя гибели инфицированных клеток. В результате скоординированного взаимодействия врожденного и приобретенного иммунитета пиковые реакции Т- и В-клеток приводят к снижению вирусной нагрузки и ослаблению воспаления, часто в течение одной недели после заражения.
T- и B-клетки памяти
После удаления вируса большинство эффекторных Т- и В-клеток погибают. Сохранившиеся Т-клетки становятся Т-клетками памяти. Сохранившиеся В-клетки генерируют либо долгоживущие плазматические клетки, продуцирующие антитела, либо становятся В-клетками памяти. Клетки памяти способны быстро реагировать на повторное заражение.
SARS-CoV-2-специфические CD4+ и CD8+ Т-клетки обнаруживаются в кровотоке как у активно инфицированных, так и у выздоровевших пациентов, что свидетельствует о потенциальной способности развития защитного клеточного иммунитета.
Т-клетки памяти бывают:
- эффекторными – реагирующими при высоких титрах вируса;
- центральными – служащими резервуаром для защиты во время будущих реинфекций.
Т-клетки, расположенные в очагах инфекции, могут стать тканево-резидентными T-клетками памяти (TRM).
Иммунитет противовирусный
 Иммунитет противовирусный — раздел учения об иммунитете, раскрывающий природу и особенности защитных факторов и механизмов организма человека и животных, направленных на восстановление постоянства внутренней среды организма хозяина путем распознавания вирусных агентов и подавления их биологической активности.Отличия механизмов противовирусного иммунитета от механизмов иммунитета против бактерий, объясняются выраженным своеобразием биологии вирусов как возбудителей с молекулярной неклеточной организацией, с уникальными структурой, способом размножения и патогенезом вызываемых заболеваний. Такие симптомы, как беспричинный кашель у ребенка без температуры или ломота в теле без внешних проявлений, могут являться проявлениями отсутствия противовирусного иммунитета.Приобретенный противовирусныйиммунитетсвязан как с участием специфических факторов (В- лимфоциты, продуцирующие антитела классов G, М, А, Е; Т-лимфоциты и макрофаги, разрушающие зараженные вирусами клетки и стимулирующие В-лимфоциты), так и неспецифических факторов (интерферон, неспецифические ингибиторы). От этих основных и первичных гуморальных и клеточных механизмов И. п. следует дифференцировать факторы, регулирующие физиол. активность В- и Т-лимфоцитов и макрофагов, но не влияющие непосредственно на подавление репродукции вирусов (возрастные, нейрогуморальные факторы, витамины, гормоны).
Иммунитет противовирусный — раздел учения об иммунитете, раскрывающий природу и особенности защитных факторов и механизмов организма человека и животных, направленных на восстановление постоянства внутренней среды организма хозяина путем распознавания вирусных агентов и подавления их биологической активности.Отличия механизмов противовирусного иммунитета от механизмов иммунитета против бактерий, объясняются выраженным своеобразием биологии вирусов как возбудителей с молекулярной неклеточной организацией, с уникальными структурой, способом размножения и патогенезом вызываемых заболеваний. Такие симптомы, как беспричинный кашель у ребенка без температуры или ломота в теле без внешних проявлений, могут являться проявлениями отсутствия противовирусного иммунитета.Приобретенный противовирусныйиммунитетсвязан как с участием специфических факторов (В- лимфоциты, продуцирующие антитела классов G, М, А, Е; Т-лимфоциты и макрофаги, разрушающие зараженные вирусами клетки и стимулирующие В-лимфоциты), так и неспецифических факторов (интерферон, неспецифические ингибиторы). От этих основных и первичных гуморальных и клеточных механизмов И. п. следует дифференцировать факторы, регулирующие физиол. активность В- и Т-лимфоцитов и макрофагов, но не влияющие непосредственно на подавление репродукции вирусов (возрастные, нейрогуморальные факторы, витамины, гормоны).
Отличия защитных факторов противовирусногоиммунитета определяются особенностями биологии и взаимодействия вирусов с чувствительными клетками, устойчивостью вирусов к внутриклеточным энзимам и высокой лабильностью к физиол. температуре тела теплокровных хозяев.
Своеобразие противовирусногоиммунитета связано в основном с важной защитной ролью факторов клеточной резистентности, интерферона, место секреторного иммунитета, несценических гуморальных (3-ииги торов и термической денатурации). При противовирусномиммунитете меньшее значение, чем при антибактериальном иммунитете, имеет фагоцитоз, направленный в основном на захватывание зараженных клеток и изоляцию находящихся там вирусов и их токсических продуктов
Механизмы гуморальной и клеточной специфической защиты при противовирусномиммунитете и антибактериальном иммунитете имеют менее существенные отличия.
Последние информационные материалы :: Все материалы
- Осмотр полости рта: симптомы заболеваний
- Избавление от простатита по-американски
- Половые расстройства
- Ангина — симптомы и лечение
- Почему ухудшается зрение
- Правила хранения сцеженного грудного молока
- Анестезия для лечения зубов во время беременности
- Гонорея — молчаливая проблема
- Социальная фобия, ее понятие, признаки и методы лечения
- Жировой гепатоз печени и его лечение
Что еще?
Желающий оставаться здоровым человек никогда не откажется от отпуска и не станет проводить его в родном городе. Главная особенность поездок на курорты и путешествий в другие страны в том, что они действуют на организм подобно мумие с прополисом – заставляют его «включить» биологический резерв для приспособления к новым окружающим условиям. Прибегать к ним чаще 2 раз в год не стоит, но один – обязательно нужно.
Поддержать здоровье помогут и простейшие методы закаливания:
- контрастный душ утром;
- обливания прохладной водой с растиранием грубым полотенцем;
- прогулки не меньше часа на ночь и утренние пробежки, даже пусть вялой рысцой;
- посещение сауны и солярия, если нет патологий сердца или сосудов.
Часто болеющим ОРВИ пациентам стоит чаще бывать летом в хвойном лесу, а зимой – в соляной комнате.
Оцените, пожалуйста, статью:
Нравится1Не нравится1
Main Article Content
Aбдуллaев Aкобур Эшмaмaт угли
Термезский филиaл Тaшкентской медицинской aкaдемии
abdullayevakobir64@gmail.com
Тожиев Шaхзод Эшмурaт угли
Термезский филиaл Тaшкентской медицинской aкaдемии
stojiyev57@gmail.com
Жумaниёзовa Юлдуз Отaбековнa
Термезский филиaл Тaшкентской медицинской aкaдемии
yulduzjumaniyozova1224@gmail.com
Кaримов Ботирбек Aбдисобир угли
Термезский филиaл Тaшкентской медицинской aкaдемии
kbobur18@gmail.com
Нaмозов Мaхмуд Мaмaшукурович
Термезский филиaл Тaшкентской медицинской aкaдемии.
maxmudnamozov571@gmail.com
Аннотация:
В стaтья рaссмотрен принцип обрaзовaния нa молекулярно-клеточном уровне противовирусного иммунитетa, формирующего с помощью клеточных рецепторов и медиaторов межклеточного взaимодействия (интерлейкинов) aдеквaтный ответ aктивности инфекционного процессa. Предстaвлены клеточные мехaнизмы, зaнимaющие центрaльное место в формировaнии противовирусного иммунитетa, связaнные, глaвным обрaзом, с внутриклеточным действием вирусов и обеспеченные функционaльной aктивностью специфических цитотоксических Т-лимфоцитов, Т-эффекторов и мaкрофaгов. Подробно рaссмотрены основные фaзы гуморaльного мехaнизмa противовирусного иммунного ответa, формы учaстия aнтител в отношении вирионов, нaходящихся внеклеточно. Aнaлиз действия комплексa неспецифических фaкторов резистентности и aдaптивного иммунитетa оргaнизмa человекa с учетом модификaции пaтогенезa вирусной инфекции должен привести к лучшему понимaнию путей взaимодействия вирусов с оргaнизмом человекa, особенностей противостояния иммунной системы оргaнизмa aтaке вирусов и формировaния противовирусного иммунитетa.
Взаимодействие генетического материала вирусов с организмом
Процесс взаимодействия генетического материала вирусов с организмом начинается с проникновения вируса в клетку. Это происходит через различные пути, такие как проникновение через поврежденную клеточную мембрану или в результате активного внедрения в клетку с помощью специальных белков на поверхности вируса.
После проникновения в клетку, генетическое материало вируса начинает взаимодействовать с клеточными компонентами организма. В случае вирусов с ДНК, генетический материал вируса интегрируется в геном клетки-хозяина и может оставаться там в течение длительного времени. Это может привести к развитию хронической инфекции или даже к возникновению рака. В случае вирусов с РНК, генетическое материало вируса используется для синтеза вирусных белков и РНК, которые затем собираются в новые вирусы.
Организм реагирует на вирусное заражение различными способами. Один из главных механизмов защиты — это иммунитет, который активируется при вирусной инфекции. Иммунитет может быть основан на антителах, которые связываются с вирусами и помогают клеткам иммунной системы уничтожить их. Также существует клеточный иммунитет, при котором определенные клетки иммунной системы, такие как цитотоксические Т-лимфоциты, распознают и уничтожают инфицированные клетки.
Тип вирусаГенетическое материалоПримеры
| Вирусы ДНК | ДНК | Герпесвирусы, папилломавирусы |
| Вирусы РНК | РНК | Грипповирусы, коронавирусы |
Взаимодействие генетического материала вирусов с организмом является сложным процессом, который может иметь различные последствия для здоровья человека. Понимание этого взаимодействия и механизмов защиты организма помогает разрабатывать эффективные методы борьбы с вирусами и предотвращать их распространение.
Вирусные уловки против иммунитета человека: как вирусы обходят иммунную защиту?
На каждом этапе противовирусной защиты человека вирусы находят лазейки, чтобы эту защиту обойти. Как они это делают?
Основных принципов борьбы с возбудителями вирусной инфекции у человеческого иммунитета два: это проверка гистосовместимости и целенаправленный поиск инфекций. Первое соответствует специфическому (врождённому) иммунитету, второе – неспецифическому (адаптивному).
К каждому из этих подходов вирусы пытаются найти ключик. В первом случае вирусы учатся отменять проверку ГКГС, чтобы заражённая клетка не попала под уничтожающий залп естественного киллера. На это, в частности, способны вирусы гепатита B и C, и именно поэтому их так трудно подавить.
Во втором случае вирусы проявляют больше фантазии:
- блокируют выработку интерферонов, препятствуя эффективному иммунному ответу,
- мутируют быстрее, чем Т-хелперы успевают собирать антигены и менять «ориентировки» В-лимфоцитов и Т-киллеров,
- подавляют функцию костного мозга – выработку лимфоцитов, моноцитов и др. иммунных клеток,
- провоцируют реакции иммунной гиперчувствительности.
О последнем хотелось бы остановиться чуть подробнее, поскольку именно с этим механизмом связано явление цитокинового шторма, который ассоциируют и с коронавирусом SARS-CoV-2 в том числе.
Всего типов реакций иммунной гиперчувствительности четыре: анафилактический, цитотоксический, иммунокомплексный и замедленного типа. Вирусы, как правило, вызывают реакции II и III типа, вплоть до тяжёлых жизнеугрожающих состояний.
Когда вирус предъявляет клеткам антигены, похожие на собственные антигены организма, то под перекрёстный огонь иммунитета, подогретого вирусной атакой, начинают попадать ни в чём не повинные клетки организма хозяина.
А может положить начало порочному кругу цитокинового шторма. Запустилось воспаление,→ произошёл выброс цитокинов, → те усилили воспаление, → оно спровоцировало ещё больший выброс цитокинов, и так либо до момента, пока не будет применена контролируемая иммуносупрессия, либо без лечения всё кончится летальным исходом.
При этом пациент погибает не от вирусной инфекции как таковой, а от разбушевавшегося иммунитета, который вышел из-под контроля и применил к организму тактику выжженной земли.
Также встречается антирецепторный вариант реакции иммунной гиперчувствительности II типа, когда антитела присоединяются к рецепторам клеток и блокируют определённые нейроэндокринные реакции.
Например, такую картину мы наблюдаем при тиреотоксикозе, когда антитела не дают тиреотропному гормону ингибировать функцию щитовидной железы, и начинается её неконтролируемый разгон. Сходная картина наблюдается при миастении.
Реакция III типа характеризуется присоединением больших иммунокомплексов IgG и IgM не к иммунным клеткам, а, например, к клеткам сосудов, после чего элиминируются с повреждением наших собственных тканей.
Чтобы подобных вещей не происходило, пациентам, конечно же, не следует заниматься попытками раззадорить и подбодрить иммунитет без наблюдения врача.
Даже пониженная функция иммунной системы не всегда указывает на необходимость иммуностимуляции. Порой с иммунитета просто нужно снять тормоза, навешанные нездоровым образом жизни пациента, чтобы система заработала нормально.
Для этого давайте разберёмся, на что уходят ресурсы иммунной системы. Чем она оказывается занята и какой ценой ей даётся приведение организма в порядок после наших отнюдь не человеколюбивых экспериментов над собой.
Иммуномодуляторы на натуральной основе
Помимо эхинацеи, используются и другие средства для повышения иммунитета. Противовирусными свойствами обладают не менее эффективные:
- Настойка элеутерококка – курс прием для взрослых составляет 30 дней. Лекарство не просто укрепляет организм, но и придает жизненных сил, бодрости.
- Настойка корня женьшеня. Производит аналогичный терапевтический эффект, но в отличие от экстракта элеутерококка, имеет ряд ограничений к применению.
- Настойка лимонника китайского. Повышает стрессоустойчивость и укрепляет иммунитет, делая организм устойчивым к ОРВИ в период массовой заболеваемости.
Основные средства для укрепления иммунитета
Для усиления свойств противовирусного иммунитета, необходимых для борьбы с различными инфекциями, фармакологическая отрасль занимается разработкой лекарственных препаратов, относящихся к категории противовирусных и иммуностимулирующих. Вне зависимости от причины ослабления иммунитета, выбор такого медикамента следует доверять врачу-иммунологу. На сегодняшний день выпускаются иммуномодулирующие средства в различных лекарственных формах для взрослых и детей.
Классифицируют их следующим образом:
- стимуляторы натурального происхождения;
- препараты на бактериальной основе;
- биогенные стимуляторы;
- индукторы выработки интерферонов человека;
- лекарства животного происхождения (из вилочковой железы крупного рогатого скота);
- адаптогенные иммуномодуляторы;
- синтетические препараты.
Что определяет эффективность приобретенного иммунного ответа
Когда приобретенные иммунные ответы на инфекцию неоптимальны или вирус развил средства для уклонения от иммунных ответов (включая подавление вирусом иммунитета), может наступить хроническая инфекция или системное заболевание и смерть, особенно у лиц из группы риска. Тяжесть заболевания при коронавирусе SARS-CoV-2 различна. Поэтому необходимо понимать, какие факторы определяют эффективность приобретенного иммунного ответа и длительный защитный иммунитет, особенно в уязвимых группах населения: пожилых и людей с ослабленным иммунитетом.
Ключевой фактор в устранении вирусных инфекций – устойчивые высокоэффективные противовирусные реакции Т- и В-клеток. Наивные Т- и В-клетки имеют на поверхности разнообразные рецепторы вирусного распознавания, поэтому могут распознавать широкий диапазон вирусов. Во время инфекции отбираются T-клетки с наиболее подходящими T-клеточными рецепторами – они обладают большей способностью связывать вирусные пептиды. Сродство B-клеточных рецепторов к вирусным белкам продолжает увеличиваться в ходе инфекции через процессы соматической гипермутации и клональной экспансии. Соматическая гипермутация – механизм, обеспечивающий разнообразие B-клеточных рецепторов и антител. Благодаря ему иммунная система может распознавать больше различных патогенов. Клональная экспансия – процесс деления B-клеток, при котором из одной клетки появляется множество копий.
B-клетки переключаются с раннего синтеза антител класса M (IgM) на синтез антител IgG и IgA с более высоким сродством. Эти антитела обнаруживаются в сыворотке выздоравливающих пациентов с COVID-19.
Величина ранних ответов антител может свидетельствовать о тяжести инфекции, поскольку более высокие титры антител IgM и IgG ассоциированы с более тяжелым заболеванием. Как и в случае с другими вирусными инфекциями, общие титры антител к SARS-CoV-2 в сыворотке крови уменьшаются после излечения активной инфекции. Однако долгоживущие В-клетки памяти могут сохраняться и продуцировать циркулирующие вируснейтрализующие антитела. Недавнее исследование показало, что через 6-8 месяцев после начала заболевания COVID-19 нейтрализующие антитела против SARS-CoV-2 были обнаружены у 90% выздоровевших пациентов. Также важно отслеживать и сравнивать продолжительность реакции В-клеток памяти на естественную инфекцию SARS-CoV-2 и вакцины





























